
Wetenschap
Wanneer waterstof zuurstof ontmoet:de krachtige exotherme reactie die water vormt
Door Clare Jackson | Bijgewerkt op 30 augustus 2022
Zolnierek/iStock/GettyImages
TL;DR
Waterstof en zuurstof combineren explosief om water te vormen, waarbij een aanzienlijke hoeveelheid warmte vrijkomt.
Waterstof- en zuurstofmix
Bij omgevingstemperatuur bestaan waterstof- (H₂) en zuurstof- (O₂)-gassen naast elkaar zonder te reageren, omdat hun moleculen onvoldoende kinetische energie missen om bestaande bindingen tijdens botsingen te verbreken. Het mengsel is stabiel totdat een externe energiebron de reactie in gang zet.
Activeringsenergie
Het introduceren van een vonk of hitte verhoogt de temperatuur van sommige moleculen, waardoor hun botsingsenergie toeneemt. Zodra de energie de bescheiden activeringsdrempel voor waterstof overschrijdt (ongeveer 0,3 eV per binding), vormen de H₂- en O₂-moleculen nieuwe covalente bindingen, waardoor water ontstaat.
Exotherme reactie
Waterstof en zuurstof bezitten een hogere interne energie dan de resulterende watermoleculen. Bijgevolg komt bij de reactie energie vrij in de vorm van warmte, licht en geluid. De exotherme aard veroorzaakt een kettingreactie, waardoor de verbranding zich snel door het resterende mengsel voortplant.
Elektronengedrag
Op elektronisch niveau delen waterstofatomen hun afzonderlijke elektronen om de binnenste schil van twee elektronen te vullen, terwijl zuurstofatomen vier elektronen delen om hun buitenste schil van acht te voltooien. De meest stabiele opstelling wordt bereikt wanneer twee waterstofatomen elk één elektron delen met een enkel zuurstofatoom, waardoor het H₂O-molecuul ontstaat. Deze herschikking maakt het energieverschil vrij dat de reactie voedt.
Producten
De primaire producten zijn water (H₂O) en warmte. De vrijkomende warmte kan worden benut voor werkzaamheden, zoals het aandrijven van turbines, hoewel de reactie onder normale omstandigheden in wezen onomkeerbaar is.
 Bovenste en onderste plaatcontroles op de Tohoku-oki-aardbeving in 2011
Bovenste en onderste plaatcontroles op de Tohoku-oki-aardbeving in 2011 Hoe is de aardewetenschap gerelateerd aan de echte wereld?
Hoe is de aardewetenschap gerelateerd aan de echte wereld?  Hoe onderscheid te maken tussen een mannelijke en vrouwelijke mus
Hoe onderscheid te maken tussen een mannelijke en vrouwelijke mus Misschien vindt u een zeldzame soort in uw achtertuin:hoe mondiale burgerwetenschap bijdraagt aan kennis over biodiversiteit
Misschien vindt u een zeldzame soort in uw achtertuin:hoe mondiale burgerwetenschap bijdraagt aan kennis over biodiversiteit  De impact van klimaatverandering op het stroomgebied van de Tana in Kenia
De impact van klimaatverandering op het stroomgebied van de Tana in Kenia
Hoofdlijnen
- Hoe zijn ribosomen gerelateerd aan objecten voor het dagelijkse leven?
- Wat is een micostaat?
- Wat is een wetenschapper die levenscycli bestudeert?
- Chromosoomorganisatie komt voort uit 1-D-patronen
- Wat zijn de drie delen van de celtheorie en wie heeft ze geschreven?
- Waarom is genetische recombinatie belangrijk?
- Correct gebruikte neonaten hebben geen nadelige invloed op bijenvolken, nieuwe onderzoeksresultaten
- Welke plant produceert veel sporen die worden verspreid door wind of water?
- Hoe verschilt gametogenese van mannen dan van vrouwen?
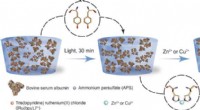
- Kation-geïnduceerde vormprogrammering en morphing in op eiwit gebaseerde hydrogels
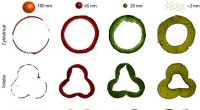
- Fluorescerende breathalyzer maakt optimalisatie van katalysatoren veel gemakkelijker
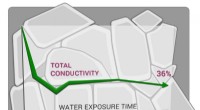
- Wetenschappers tonen aan dat een veelbelovende vaste elektrolyt hydrofoob is
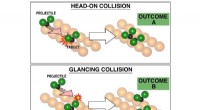
- Chemici bevorderen het vermogen om chemische reacties te beheersen
- Een concrete stap in de richting van nul CO2-uitstoot bij de cementproductie

 Welke energie Quanta werd ontdekt door Max Planck?
Welke energie Quanta werd ontdekt door Max Planck?  Wiskundige stelt methode voor om het wiskundige model van stofoverdracht door een celwand te vereenvoudigen
Wiskundige stelt methode voor om het wiskundige model van stofoverdracht door een celwand te vereenvoudigen Kan een object een constante snelheid hebben en maar variabele snelheid?
Kan een object een constante snelheid hebben en maar variabele snelheid?  Hoe weet u of een object de meeste potentiële energie heeft?
Hoe weet u of een object de meeste potentiële energie heeft?  Wat is de chemische formule voor verbindingen die om de twee chlooratomen één zinkatoom bevatten?
Wat is de chemische formule voor verbindingen die om de twee chlooratomen één zinkatoom bevatten?  Hoe een smederij te bouwen
Hoe een smederij te bouwen  Kun jij ontsnappen aan de zwaartekracht?
Kun jij ontsnappen aan de zwaartekracht?  Wat bepaalt de vorm en het volume van een gas in continer?
Wat bepaalt de vorm en het volume van een gas in continer?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

