
Wetenschap
Titratieberekeningen beheersen:een praktische gids voor nauwkeurige concentratiebepaling
Door Claire Gillespie
Bijgewerkt op 30 augustus 2022
Een titratie is een nauwkeurige analytische techniek die wordt gebruikt om de concentratie van een onbekende oplossing te bepalen door deze te laten reageren met een oplossing met een bekende concentratie. Door het volume titrant te meten dat nodig is om het eindpunt van de reactie te bereiken, kunnen scheikundigen met vertrouwen de molariteit van de analyt berekenen.
Essentiële uitrusting
- Titrant (oplossing met bekende concentratie)
- Analiet (onbekende oplossing)
- Erlenmeyer
- Buret
- Zuur-base-indicator
- Wetenschappelijke rekenmachine of spreadsheet
Stap 1:uw apparaat instellen
Plaats de analyt in een erlenmeyerkolf. Monteer de titrant in een buret, zorg ervoor dat de kraan goed afgesloten is en dat de volume-indicator helder is.
Stap 2:Voer de titratie uit
Voeg de titrant langzaam toe aan de analyt terwijl u voorzichtig ronddraait. Voeg een paar druppels van een geschikte indicator toe:fenolftaleïne verandert bijvoorbeeld van roze in basische oplossingen naar kleurloos in zure omstandigheden. Het eindpunt wordt gemarkeerd door een permanente kleurverandering.
Stap 3:Pas de Molariteitsformule toe
Voor een stoichiometrische relatie van 1:1 is de berekening eenvoudig:
\[\text{M}_{\text{titrant}}\times V_{\text{titrant}} =\text{M}_{\text{analyte}}\times V_{\text{analyte}}\]
Als de verhouding verschilt, neem dan de stoichiometrische factor op. Als u bijvoorbeeld de concentratie NaOH in een monster van 25 ml wilt bepalen met behulp van 35 ml 1,25 M HCl (verhouding 1:1), berekent u:\[\text{M}_{\text{NaOH}} =\frac{1.25\,\text{M}\times35\,\text{mL}}{25\,\text{mL}} =1,75\,\text{M}\]
Waarom titraties belangrijk zijn
Titraties zijn van fundamenteel belang in laboratoria over de hele wereld, waardoor nauwkeurige kwantificering van zuren, basen en andere reactieve soorten mogelijk is. Ze zijn van cruciaal belang bij farmaceutische producten, milieutests en kwaliteitscontrole en zorgen ervoor dat producten voldoen aan strenge veiligheids- en werkzaamheidsnormen.
Beknopte referentie
Gebruik de molariteitsvergelijking 1:1 voor de meeste zuur-basetitraties. Pas de stoichiometrie aan bij het omgaan met polyprotische zuren of complexe ionen.
 Chemische verandering:definitie, voorbeelden en toepassingen in de echte wereld
Chemische verandering:definitie, voorbeelden en toepassingen in de echte wereld  Vloeibare broom- en stikstof levert een tribromide -formule op?
Vloeibare broom- en stikstof levert een tribromide -formule op?  Nieuwe milieuvriendelijke synthesemethode maakt gebruik van aluminiumoxide als recyclebare katalysator
Nieuwe milieuvriendelijke synthesemethode maakt gebruik van aluminiumoxide als recyclebare katalysator Wat is het gas geëvolueerd wanneer ammoniumchloride en natriumnitraat aan elkaar worden verwarmd?
Wat is het gas geëvolueerd wanneer ammoniumchloride en natriumnitraat aan elkaar worden verwarmd?  Nieuwe strategie voor kristaltechnologie om ultraheldere fluorescerende vaste kleurstoffen te ontwerpen
Nieuwe strategie voor kristaltechnologie om ultraheldere fluorescerende vaste kleurstoffen te ontwerpen
 Fossielen tonen aan dat er 66 miljoen jaar lang insecten zijn geweest die kauribomen aten
Fossielen tonen aan dat er 66 miljoen jaar lang insecten zijn geweest die kauribomen aten  Gravende zoogdieren graven voor de kost, maar hoe doen ze dat?
Gravende zoogdieren graven voor de kost, maar hoe doen ze dat?  Easy Ecology Experiments for Kids
Easy Ecology Experiments for Kids Wat moet er worden toegepast om een object van richting te laten veranderen?
Wat moet er worden toegepast om een object van richting te laten veranderen?  Menselijke geografie is de definitie van de menselijke ecologie door wie?
Menselijke geografie is de definitie van de menselijke ecologie door wie?
Hoofdlijnen
- Eenheid in de cel waarin DNA is verdeeld en verpakt?
- Welke levende wezens bestaan uit slechts één cel?
- In welke tak van de wetenschap is gelotologie?
- Hoe heet de lagere structuur van mensen?
- Welke celtypen zitten in het nerveuze weefsel?
- De vitale rol van ontbinders in de gezondheid van ecosystemen
- Hoe kan een organisme zich voortplanten zonder een partner?
- Wiskunde laat zien hoe ziekten zich ontwikkelen en hoe bacteriën resistentie tegen geneesmiddelen ontwikkelen
- Biologen ontdekten de paden van groepen van de lophopoor
- Biochemici duiken in de gezondheidsvoordelen van olijven en olijfolie

- Stabiele toevoer van elektrochroom metallo-supramoleculaire polymeer

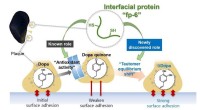
- Hoe mosselen hun hechting onder water behouden
- Maskers slimmer en veiliger maken tegen COVID-19
- Binnen een atoom:de locaties van protonen, neutronen en elektronen

 Dankzij een krachtige nieuwe techniek kunnen wetenschappers bestuderen hoe eiwitten in cellen van vorm veranderen
Dankzij een krachtige nieuwe techniek kunnen wetenschappers bestuderen hoe eiwitten in cellen van vorm veranderen  Wat zijn 4 soorten niet -mechanische energie?
Wat zijn 4 soorten niet -mechanische energie?  Een tektonische plaat is een ander woord voor een continent?
Een tektonische plaat is een ander woord voor een continent?  Zeegrasherstel beter bestand maken tegen stijgende temperaturen met behulp van generalistische grassen
Zeegrasherstel beter bestand maken tegen stijgende temperaturen met behulp van generalistische grassen  Onderzoekers en supercomputers helpen bij het interpreteren van de nieuwste LIGO-bevindingen
Onderzoekers en supercomputers helpen bij het interpreteren van de nieuwste LIGO-bevindingen Wat hebben bacteriën gemeen met cellen en andere levende organismen?
Wat hebben bacteriën gemeen met cellen en andere levende organismen?  Wat is een wrijvende kracht die werkt tegen de beweging tussen twee ontroerende oppervlakken en altijd een object vertraagt?
Wat is een wrijvende kracht die werkt tegen de beweging tussen twee ontroerende oppervlakken en altijd een object vertraagt?  Wat zijn enkele kenmerken van Joviaanse planeten?
Wat zijn enkele kenmerken van Joviaanse planeten?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

