
Wetenschap
Huishoudelijke basissen die u elke dag gebruikt – van zuiveringszout tot loog
Zuiveringszout, borax, ammoniak, loog en andere huishoudelijke basissen
Door Lauren Whitney | Bijgewerkt op 30 augustus 2022
Voor een scheikundige is een base een elektronenpaardonor. In alledaagse termen is het de alkalische tegenhanger van een zuur, en wanneer de twee elkaar ontmoeten, neutraliseren ze elkaar. De pH-schaal, variërend van 0 tot 14, wijst elke stof met een pH hoger dan 7 als base toe. Hoewel het woord ‘basis’ misschien technisch klinkt, zijn de materialen zelf gebruikelijk in de meeste keukens, badkamers en wasruimtes.
Zuiveringszout (natriumbicarbonaat)
Zuiveringszout (NaHCO3 ) heeft een pH van 8,3, licht alkalisch vergeleken met gedestilleerd water (pH7,0). Het is een belangrijk onderdeel bij het bakken, waar het reageert met zuren om het deeg op te tillen. Buiten de oven ontgeurt het afvoerkanalen, reinigt het oppervlakken en dient het als een zacht, niet-giftig schuurmiddel. Een theelepel in een kopje water produceert de karakteristieke gladheid van een basis, en een kleine dosis kan de milde maagzuurgraad verzachten. Omdat het veilig is om aan te raken, is baking soda een ideaal huishoudelijk schoonmaakmiddel.
Borax (natriumtetraboraatdecahydraat)
Historisch gebruikt om mummies te bewaren, borax (Na2 B4 O7 ·10H2 O) komt nu voor in wasmiddelen en ongediertebestrijdingssprays. De pH van 9,2 maakt het 920 keer alkalischer dan zuiver water. Wanneer borax is opgelost, komen er boraationen vrij die zich met zuurstof verbinden en waterstofperoxide vormen, waardoor het milde desinfecterende en blekende eigenschappen heeft. Hoewel contact met de huid irritatie kan veroorzaken, is borax bij inslikken licht giftig en moet het daarom buiten het bereik van kinderen worden bewaard.
Melk van Magnesia (Magnesiumhydroxide)
Milk of Magnesia is een klassiek maagzuurremmer en laxeermiddel. De poedervorm van magnesiumhydroxide (Mg(OH)2 ) ziet er melkachtig uit en heeft een pH van 10,5. Commerciële producten maskeren vaak de bittere smaak van alkaliën met munt- of fruitsmaken, maar de onderliggende chemie blijft hetzelfde:een base die overtollig maagzuur neutraliseert.
Ammoniak (ammoniumhydroxide)
In een huishoudelijke omgeving verwijst ‘ammoniak’ gewoonlijk naar een 5-10% oplossing van ammoniumhydroxide (NH4 OH), een heldere vloeistof met een pH van 11. Het is een krachtige reiniger die vet en vuil op vrijwel elk oppervlak oplost. Hoewel in sommige frisdranken sporen van ammoniak kunnen voorkomen, kun je het het beste alleen gebruiken:als je het met andere schoonmaakmiddelen mengt, kunnen er giftige dampen ontstaan.
Loog (natriumhydroxide)
Loog, of natriumhydroxide (NaOH), is de sterkste base die algemeen verkrijgbaar is voor thuisgebruik. De pH is hoger dan 13 en wordt gebruikt in afvoerreinigingsmiddelen, ovenreinigers en zelfs in het traditionele proces waarbij maïs in korrels wordt omgezet. Omdat loog bijtend is, kan het ernstige chemische brandwonden op de huid en ogen veroorzaken; Draag altijd handschoenen en oogbescherming bij het hanteren.
 Statistische gevolgtrekking om de werkwijze van een zeer ervaren kristallograaf na te bootsen
Statistische gevolgtrekking om de werkwijze van een zeer ervaren kristallograaf na te bootsen Welke methode is het meest geschikt voor het scheiden van een mengsel van natriumchloride en jodium?
Welke methode is het meest geschikt voor het scheiden van een mengsel van natriumchloride en jodium?  Gebruik van metaal-organische kaders om plastic af te breken
Gebruik van metaal-organische kaders om plastic af te breken Glutamine-afhankelijke activering van celgroei ontdekt
Glutamine-afhankelijke activering van celgroei ontdekt Waarom verandert de kleur van kopersulfaat als je er een ijzeren spijker in doopt?
Waarom verandert de kleur van kopersulfaat als je er een ijzeren spijker in doopt?
 Water is mogelijk schaars voor nieuwe energiecentrales in Azië
Water is mogelijk schaars voor nieuwe energiecentrales in Azië IJs in beweging:satellieten zien tientallen jaren van verandering
IJs in beweging:satellieten zien tientallen jaren van verandering Wat is principe?
Wat is principe?  Bepalen wanneer India in botsing kwam met Azië om de Himalaya-bergen te vormen
Bepalen wanneer India in botsing kwam met Azië om de Himalaya-bergen te vormen Wat is de term die wordt gebruikt om een verklaring te beschrijven van een natuurlijk fenomeen dat wordt ondersteund door observatie en experimenten?
Wat is de term die wordt gebruikt om een verklaring te beschrijven van een natuurlijk fenomeen dat wordt ondersteund door observatie en experimenten?
Hoofdlijnen
- Waarom komen wetenschappers op het gebied van wetenschapsgebied?
- Gepolariseerde microscopietechniek toont nieuwe details van hoe eiwitten zijn gerangschikt
- Wat is celdifferentiatie en specialisatie?
- Wat zorgt ervoor dat vliegen aanvallen?
- Hoe gaan ziekten van de ene soort naar de andere?
- Is het waar dat het lichaam van een schimmel meestal bestaat uit veel gecelleerde draadachtige buizen die hyfen worden genoemd?
- Kan alle micro -organisme worden gekweekt met behulp van synthetische media?
- Wat is Hermisphere?
- Wat is het micro -organisme dat betrokken is bij het maken van Bagoong?
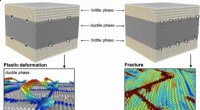
- Voorgestelde technische methode kan gebouwen en bruggen veiliger maken
- Baanbrekende nieuwe herbruikbare lijm werkt onder water

- Team ontwikkelt productieproces voor biobrandstof in samenwerking met Noord-Amerikaanse onderzoekers
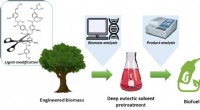
- Diepeutectische oplosmiddelen vervangen vervuilende industriële oplosmiddelen

- Superstaalproject bereikt grote doorbraak

 Bijtanken van satellieten in de ruimte met behulp van een robot
Bijtanken van satellieten in de ruimte met behulp van een robot Hoe computeralgoritmen onze ervaring van de echte wereld vormgeven
Hoe computeralgoritmen onze ervaring van de echte wereld vormgeven  Wat gebeurt er met ionen nadat zout water verdampt?
Wat gebeurt er met ionen nadat zout water verdampt?  Welk aardewerkvorm ontleent zijn naam aan het Italiaans voor de aarde?
Welk aardewerkvorm ontleent zijn naam aan het Italiaans voor de aarde?  Laboratoriumexperimenten met hoge resolutie laten zien hoe cellen 'eten'
Laboratoriumexperimenten met hoge resolutie laten zien hoe cellen 'eten'  The Difference Between Spring & Neap Tides
The Difference Between Spring & Neap Tides Kun je me een wetenschapsproject geven voor de 6e klasser?
Kun je me een wetenschapsproject geven voor de 6e klasser?  Wat voor soort rotsen heeft West Virginia?
Wat voor soort rotsen heeft West Virginia?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

