
Wetenschap
Kaliumpermanganaat:formule, eigenschappen en praktisch gebruik
Kaliumpermanganaat (KMnO4 ) is een veelgebruikt oxidatiemiddel dat bekend staat om zijn opvallende dieppaarse tint en sterke redoxpotentieel. Bij reductie verliest de verbinding zijn karakteristieke kleur en wordt kleurloos, waardoor het een uitstekende indicator is voor titraties en analytische chemie.
Geschiedenis
Kaliumpermanganaat, ontdekt in 1659, werd al snel een belangrijk onderdeel van de vroege fotografische verwerking, waarbij het kleurvermogen ervan werd gebruikt om zwart-witdia's te ontwikkelen. Tegenwoordig blijft het relevant in de fotografie, vooral bij de ontwikkeling van monochrome beelden, en is het uitgebreid naar medische en industriële toepassingen.
Chemische componenten van de formule
KMnO4 bestaat uit één kalium- (K), één mangaan- (Mn) en vier zuurstofatomen (O) per molecuul. De molfracties zijn 1/6 voor K, 1/6 voor Mn en 2/3 voor O, wat de dominantie van zuurstof in de samenstelling van de verbinding onderstreept.
Kation- en anioncomponenten van de formule
In een waterige oplossing dissocieert kaliumpermanganaat in een kaliumkation (K + ) en een permanganaatanion (MnO4 – ). Het kaliumion is bij de meeste reacties grotendeels inert en fungeert als toeschouwer, terwijl het permanganaat-anion de actieve oxiderende soort is die verantwoordelijk is voor de chemische reactiviteit van de verbinding.
Oxidatietoestanden in de formule
Het mangaanatoom in KMnO4 heeft een oxidatietoestand van +7, waardoor het een krachtige oxidator is. Bij redoxreacties wordt mangaan gereduceerd tot een +2-toestand, waarbij vaak Mn 2+ ontstaat ionen. De zuurstofatomen behouden een oxidatietoestand van −2 en kalium blijft op +1, waardoor de algehele neutraliteit van het zout wordt gegarandeerd.
Grootte en kleur
Met een molmassa van 158,04 gmol –1 De dieppaarse kleur van kaliumpermanganaat komt voort uit d-d elektronische overgangen binnen het mangaanion, met name de beweging van een elektron naar een lege 3D-orbitaal onder blootstelling aan licht. Deze chromofore eigenschap biedt niet alleen een visuele indicatie van de concentratie, maar geeft ook aan dat hij bereid is deel te nemen aan oxidatiereacties.
 De aarde had zojuist de warmste februari ooit gemeten:rapport
De aarde had zojuist de warmste februari ooit gemeten:rapport  Economische groei stimuleren en klimaatverandering aanpakken gaan hand in hand
Economische groei stimuleren en klimaatverandering aanpakken gaan hand in hand Volkswagens overmatige uitstoot leidt tot 1, 200 vroegtijdige sterfgevallen in Europa, studie zegt:
Volkswagens overmatige uitstoot leidt tot 1, 200 vroegtijdige sterfgevallen in Europa, studie zegt: Waarom krachten elektrisch van aard zijn?
Waarom krachten elektrisch van aard zijn?  Kopers van woningverzekeringen hebben geen toegang tot openbare gegevens over overstromingen
Kopers van woningverzekeringen hebben geen toegang tot openbare gegevens over overstromingen
Hoofdlijnen
- Welk orgaan onderhoudt het water en de opgeloste homeostase?
- Wat wordt het bedoeld met haploïde en diploïd aantal chromosomen?
- Hoe creëert genetische variatie nieuwe soorten in de loop van de tijd?
- Hoe wordt in wetenschappelijk onderzoek een mogelijke verklaring genoemd?
- De meeste erfelijke informatie in de cel wordt gedragen in de ribosomen vacuoles chromosomen of Golgi-lichamen. Welke is het?
- Onderzoekers ontdekken hoe overwinterende ribosomen ontwaken
- Hetzelfde gen, verschillende paringstechnieken bij vliegen
- Wat maakt de bloedsomloop cel die vecht?
- Wat doet het controsoom in dierencel?
- Reparatie en regeneratie van perifere zenuwen mogelijk met dubbele polymeer hydrogellijm

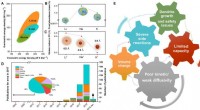
- Onderzoekers schetsen de huidige stand van zaken in de technologie van kalium-ionbatterijen
- Moeten onderwijs en communicatie over de vooruitgang van microfluïdica worden verbeterd?

- Een bijgewerkt begrip van het synthetiseren van chemicaliën met toegevoegde waarde

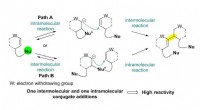
- Totale synthese van flueggenine C via een versnelde intermoleculaire Rauhut-Currier-reactie
 Hoeveel mol zwavel bevindt zich in een monster CUSO4 dat ook 3,50 x 1023 zuurstofatomen bevat?
Hoeveel mol zwavel bevindt zich in een monster CUSO4 dat ook 3,50 x 1023 zuurstofatomen bevat?  Virussen kennis ontsloten door nieuwe metagenomics-technologieën
Virussen kennis ontsloten door nieuwe metagenomics-technologieën Zijn er foto's van manen?
Zijn er foto's van manen?  Ontdekking van aminozuur onthult hoe licht huidmondjes in planten open maakt
Ontdekking van aminozuur onthult hoe licht huidmondjes in planten open maakt  Wetenschappers vinden recept voor groenere verwijdering van tuinafval
Wetenschappers vinden recept voor groenere verwijdering van tuinafval Bestrijding van online extremisme:polarisatie in sociale media en hoe het publieke gesprek te verbeteren
Bestrijding van online extremisme:polarisatie in sociale media en hoe het publieke gesprek te verbeteren Zijn 3 gallons groter dan 12 liter?
Zijn 3 gallons groter dan 12 liter?  Wat is een celschoolanalogie voor mitochondria?
Wat is een celschoolanalogie voor mitochondria?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

