
Wetenschap
Hoe het periodiek systeem te gebruiken:een praktische gids voor de basisbeginselen van de scheikunde
Door bijdrager
Bijgewerkt op 30 augustus 2022
Het begrijpen van het periodiek systeem is essentieel voor iedereen die scheikunde onderzoekt. Het laat zien hoe elk element bijdraagt aan de wereld om ons heen en laat zien hoe zelfs een eenvoudig molecuul als water kan worden verklaard via de atomaire structuur.
Stap 1 – De indeling van de tabel
Het periodiek systeem is gerangschikt door het atoomnummer te verhogen, wat het aantal protonen is (en, in een neutraal atoom, elektronen). Waterstof, het eerste element, heeft een atoomnummer van 1:één proton en één elektron. Zuurstof heeft een atoomnummer van 8, wat betekent dat er acht protonen en acht elektronen zijn. Terwijl u door de tabel beweegt, voegt u dienovereenkomstig protonen en elektronen toe.
Stap 2 – Elektronenorbitalen
Elektronen bezetten orbitalen – energiewoningen binnen een atoom. Beschouw orbitalen als verdiepingen in een appartementencomplex:de 1s-orbitaal is de begane grond (laagste energie), 2s is de eerste verdieping, 2p de tweede, 3s de derde, enzovoort. Elk orbitaaltype heeft een specifieke capaciteit en energieniveau.
Stap 3 – Orbitalen en valentie-elektronen vullen
Elektronen vullen orbitalen, beginnend met de laagste energie. Zuurstof, met acht elektronen, vult zijn orbitalen als volgt:twee in 1s, twee in 2s en vier in de 2p-set. De 2p-orbitalen kunnen zes elektronen bevatten, dus twee blijven ongepaard. Deze ongepaarde elektronen zijn de valentie-elektronen die deelnemen aan chemische bindingen.
Stap 4 – Voorbeeld van verbinding:Water (H2 O)
Waterstof heeft een enkel 1s-elektron, dat ongepaard is en beschikbaar is voor binding. Zuurstof, met twee ongepaarde elektronen, kan deze delen met twee waterstofatomen. Door elk waterstofelektron te koppelen aan een van de valentie-elektronen van zuurstof, bereikt het molecuul een stabiele configuratie zonder vrije elektronen.
Stap 5 – Elektronegativiteit
Elektronegativiteit (E-neg) meet de neiging van een element om elektronen aan te trekken. Het neemt toe van links naar rechts en van onder naar boven op de tafel, waarbij fluor het meest elektronegatieve element is. Deze eigenschap verklaart waarom waterstoffluoride (HF) een sterk zuur is:de hoge elektronegativiteit van fluor trekt het eenzame elektron op waterstof zo sterk aan dat waterstof gemakkelijk kan worden verwijderd, waardoor de zuurgraad toeneemt.
Stap 6 – Oefening baart kunst
Schets regelmatig de elektronenconfiguraties voor verschillende elementen om ongepaarde elektronen te identificeren. Als u het periodiek systeem beheerst, krijgt u een solide basis voor de hele scheikunde.
Wat je nodig hebt
- Periodiek systeem (gedrukt of digitaal)
- Basiskennis van de chemie
TL;DR (te lang; niet gelezen)
Dit artikel biedt een beknopt overzicht van atoomnummers, elektronenorbitalen, valentie-elektronen, binding en elektronegativiteit.
 Wat is het radioactieve metaal dat wordt gebruikt in de kernreactor?
Wat is het radioactieve metaal dat wordt gebruikt in de kernreactor?  Waarin wordt de dichtheid van materie uitgedrukt?
Waarin wordt de dichtheid van materie uitgedrukt?  Wat is de chemische formule voor koper II dihydrogen fosfaat?
Wat is de chemische formule voor koper II dihydrogen fosfaat?  Hygroscopische polymere gels:het verzamelen van zoet water en energie uit luchtvochtigheid
Hygroscopische polymere gels:het verzamelen van zoet water en energie uit luchtvochtigheid Is water een oxide of een hydride?
Is water een oxide of een hydride?
 Natuurkundigen lossen al lang bestaande puzzel op over hoe motten verre partners vinden
Natuurkundigen lossen al lang bestaande puzzel op over hoe motten verre partners vinden  Hoe Black & Red Ants te identificeren
Hoe Black & Red Ants te identificeren  In welke regio kan de lucht het meeste vocht vasthouden?
In welke regio kan de lucht het meeste vocht vasthouden?  Winst maximaliseren door pluimveestrooisel als meststof te gebruiken
Winst maximaliseren door pluimveestrooisel als meststof te gebruiken Microplastics in de Grote Meren:Benthisch worden
Microplastics in de Grote Meren:Benthisch worden
Hoofdlijnen
- Hoe worden organische systemen geactiveerd of gestimuleerd en ontwikkeld door activiteit?
- De hoge, natte bossen van Australië waren niet open en parkachtig toen de kolonisten arriveerden – en we zouden ze niet moeten verbranden
- Wie is de grootste wetenschapper die ooit heeft geleefd?
- Welk type binding bevat alle biologische macromoleculen bij elkaar?
- Wat zijn de organisatieniveaus in anatomie en fysiologie?
- Een somatische cel met twee van elk type chromosoom heeft een nummer?
- Vergelijk ATP met een gevonden voorwerp in uw huishouden. Wat zijn de overeenkomsten en verschillen?
- Ontbreekt de plantencel een kern?
- Lysosomen:de cellulaire compartimenten voor hydrolytische enzymen
- Nieuwe bioink brengt 3D-printen van menselijke organen dichter bij de realiteit
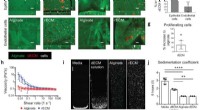
- Team gedecodeerd moleculair mechanisme dat zwermmotiliteit van bacteriële populaties remt

- Hoe bacteriën een spaarvarken creëren voor de magere tijden
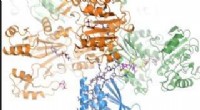
- Meest gedetailleerde röntgenfoto van batterijen tot nu toe om te laten zien waarom ze nog steeds niet goed genoeg zijn

- Polymeer afgeleid van materiaal in de schelpen van garnalen kan geneesmiddelen tegen kanker afleveren op tumorplaatsen
 Hoeveel graden zal de zon water verwarmen?
Hoeveel graden zal de zon water verwarmen?  Hoe helpen de gegevens van bewegingen van seismische golven geologen om het aardbevingsrisico voor een gebied te bepalen?
Hoe helpen de gegevens van bewegingen van seismische golven geologen om het aardbevingsrisico voor een gebied te bepalen?  Hoe is het klimaat aan de Leeward -kant van een berg verschilt van die windwaartse kant?
Hoe is het klimaat aan de Leeward -kant van een berg verschilt van die windwaartse kant?  Bemanningen vechten tegen laatste hardnekkige bosbrand in Zuid-Californië
Bemanningen vechten tegen laatste hardnekkige bosbrand in Zuid-Californië Kunnen atomen worden verdeeld in kleinere deeltjes?
Kunnen atomen worden verdeeld in kleinere deeltjes?  Hoe zie je licht van sterren miljarden jaren oud?
Hoe zie je licht van sterren miljarden jaren oud?  Waar komt alle energie in een ecosysteem oorspronkelijk vandaan?
Waar komt alle energie in een ecosysteem oorspronkelijk vandaan?  Wat is de pH van een 0,0000001 M oplossing waterstofchloride in water?
Wat is de pH van een 0,0000001 M oplossing waterstofchloride in water?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

