
Wetenschap
Vergelijking van de atomaire straal:fluor versus zuurstof - Grootteverschillen begrijpen
Dit is waarom:
* Elektronegativiteit: Fluor is het meest elektronegatieve element, wat betekent dat het een sterke aantrekkingskracht op elektronen heeft. Dit zorgt ervoor dat de elektronen dichter bij de kern worden getrokken, wat resulteert in een kleinere atoomstraal.
* Effectieve nucleaire lading: Fluor heeft een hogere effectieve nucleaire lading (de positieve lading die een elektron ervaart) vergeleken met zuurstof. Deze sterkere aantrekkingskracht tussen de kern en elektronen trekt de elektronen dichter naar elkaar toe, waardoor de atoomstraal kleiner wordt.
* Elektronenschillen: Zowel zuurstof als fluor hebben hun valentie-elektronen in de tweede elektronenschil. Fluor heeft echter nog één proton in de kern, wat de aantrekkingskracht voor elektronen vergroot, wat leidt tot een kleinere atoomstraal.
Samengevat: Hoewel zuurstof en fluor zich in dezelfde periode (rij) van het periodiek systeem bevinden, resulteren de hogere elektronegativiteit van fluor, de effectieve nucleaire lading en één extra proton in een kleinere atoomstraal vergeleken met zuurstof.
 Wat is een kenmerk van het ingrediëntenmengsel?
Wat is een kenmerk van het ingrediëntenmengsel?  Waar zijn de 4 gasplaneten van gemaakt?
Waar zijn de 4 gasplaneten van gemaakt?  Een nieuwe op suiker gebaseerde katalysator zou een potentiële oplossing kunnen bieden voor het gebruik van afgevangen koolstof
Een nieuwe op suiker gebaseerde katalysator zou een potentiële oplossing kunnen bieden voor het gebruik van afgevangen koolstof  Benzeenstructuur:een uitgebreide gids voor moleculaire binding
Benzeenstructuur:een uitgebreide gids voor moleculaire binding  Wat verklaart waarom koolstof zo’n veelzijdig element is?
Wat verklaart waarom koolstof zo’n veelzijdig element is?
 Hoe mensen multiraciale gezichten waarnemen is niet altijd zo zwart-wit, zo blijkt uit onderzoek
Hoe mensen multiraciale gezichten waarnemen is niet altijd zo zwart-wit, zo blijkt uit onderzoek  Waarom kunnen klimaten soms sterk variëren op korte afstand?
Waarom kunnen klimaten soms sterk variëren op korte afstand?  Magnetronbehandeling is een goedkope manier om zware metalen uit gezuiverd afvalwater te verwijderen
Magnetronbehandeling is een goedkope manier om zware metalen uit gezuiverd afvalwater te verwijderen Tropische storm Faxai krijgt een naam en NASA krijgt een infraroodfoto
Tropische storm Faxai krijgt een naam en NASA krijgt een infraroodfoto Wat is waar aan aardsystemen?
Wat is waar aan aardsystemen?
Hoofdlijnen
- Waar en in welke vorm wordt prokaryotisch DNA gevonden?
- Habitatverlies is de grootste bedreiging voor Australische soorten
- Wat is een archeogeneticus?
- Welk proces vindt plaats in de mitochondria van plantencellen?
- De oorsprong van het leven ontrafelen:vijf belangrijke doorbraken van de afgelopen vijf jaar
- Wat beschermt mRNA tegen aanval door cellulaire enzymen?
- Hoe verschilt de functie van celdeling in eencellige organismen van meercellige organismen?
- Uit welk type cel zijn bloedplaatjes gevormd?
- Waarom veranderen wetenschapper soms hun ideeën over het classificeren van organismen?
- Apparaat simuleert filter- en ionentransportfuncties van menselijke nieren

- Onderzoeksteams ontdekken buitengewone eigenschappen van strontiumniobaat

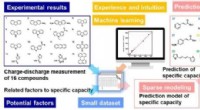
- Beste prestaties van organisch materiaal voor lithiumbatterijanode met behulp van materiaalinformatica
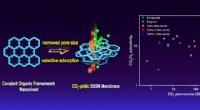
- Eenfasige covalente organische raamwerkmembranen maken CO2-selectieve scheiding mogelijk
- Mysterieus organisch uitschot verhoogt de efficiëntie van chemische reacties, kan chemisch afval verminderen
 Hoe wrijving kan worden gebruikt om elektronen over te dragen?
Hoe wrijving kan worden gebruikt om elektronen over te dragen?  Wat zijn de drie energietransformaties die plaatsvinden wanneer u een zaklamp gebruikt?
Wat zijn de drie energietransformaties die plaatsvinden wanneer u een zaklamp gebruikt?  Wat stelt het RNA in staat kern te verlaten?
Wat stelt het RNA in staat kern te verlaten?  Kan er een covalente binding ontstaan wanneer elektronen worden overgedragen tussen 2 atomen?
Kan er een covalente binding ontstaan wanneer elektronen worden overgedragen tussen 2 atomen?  Ouders aangespoord om twee keer na te denken over het kopen van Amazon Echo Dot voor kinderen
Ouders aangespoord om twee keer na te denken over het kopen van Amazon Echo Dot voor kinderen Wat is thermonoloog?
Wat is thermonoloog?  Homozygote allelcombinatie wordt weergegeven door?
Homozygote allelcombinatie wordt weergegeven door?  Nissan lanceert op China gerichte elektrische auto
Nissan lanceert op China gerichte elektrische auto
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

