
Wetenschap
Koolzuur en pH:zuur-base-chemie begrijpen
Dit is waarom:
* Koolzuur is een zwak zuur. Dit betekent dat het gedeeltelijk dissocieert in water, waarbij waterstofionen (H⁺) en bicarbonaationen (HCO₃⁻) vrijkomen.
* De aanwezigheid van meer H⁺-ionen verlaagt de pH. Een lagere pH duidt op een zuurdere oplossing.
Dus in plaats van overtollige waterstofionen te binden, draagt koolzuur feitelijk bij aan de zuurgraad van een oplossing.
Laten we eens kijken naar de chemische reactie:
H₂CO₃ ⇌ H⁺ + HCO₃⁻
Daarom zal het toevoegen van koolzuur aan een oplossing de pH verlagen en niet verhogen.
In plaats van de pH te verhogen, kun je het volgende doen:
* Een basis toevoegen: Basen zoals natriumhydroxide (NaOH) kunnen overtollige waterstofionen neutraliseren, waardoor de pH stijgt.
* Gebruik een buffersysteem: Buffersystemen zijn bestand tegen veranderingen in de pH door waterstofionen te accepteren of te doneren.
 Wat zijn de criteria bij het kiezen van een goed herkristallisatie -oplosmiddel?
Wat zijn de criteria bij het kiezen van een goed herkristallisatie -oplosmiddel?  Elektriciteit gebruiken om verontreinigende stoffen die overblijven na afvalwaterzuivering af te breken
Elektriciteit gebruiken om verontreinigende stoffen die overblijven na afvalwaterzuivering af te breken Waarom neemt het smeltpunt toe van natrium naar aluminium?
Waarom neemt het smeltpunt toe van natrium naar aluminium?  Wat is de formule om elektrochemisch equivalent te vinden?
Wat is de formule om elektrochemisch equivalent te vinden?  Nieuw inzicht in de oppervlakte-eigenschappen van tweedimensionale MXenes-materialen
Nieuw inzicht in de oppervlakte-eigenschappen van tweedimensionale MXenes-materialen
 Vee-gerelateerde antibiotica verstoren bodemecosystemen
Vee-gerelateerde antibiotica verstoren bodemecosystemen In Shawnee National Forest woedt een debat over de vraag hoe bomen het beste kunnen worden beschermd te midden van klimaatverandering en bosbranden
In Shawnee National Forest woedt een debat over de vraag hoe bomen het beste kunnen worden beschermd te midden van klimaatverandering en bosbranden  Onderzoekers:Culturele verbranding is beter voor de Australische bodem dan voorgeschreven verbranding, of helemaal geen verbranding
Onderzoekers:Culturele verbranding is beter voor de Australische bodem dan voorgeschreven verbranding, of helemaal geen verbranding  Is Earth Science de belangrijkste tak die zich bezighoudt met levende wezens?
Is Earth Science de belangrijkste tak die zich bezighoudt met levende wezens?  Russische ecologen zeggen dat Nord Stream 2 kostbaar toevluchtsoord beschadigt
Russische ecologen zeggen dat Nord Stream 2 kostbaar toevluchtsoord beschadigt
Hoofdlijnen
- Onderzoekers onthullen mechanismen van de accumulatie van organische koolstof in de bodem in verzuurde bosbodems
- Wat is de functie van fructose in planten?
- Welke cyclus produceert de meeste NADH?
- Wat zijn de verschillen tussen PCR en klonen?
- Welke soorten cellen gebruiken mitose om te delen?
- Welk molecuul bevat de erfelijke informatie voor een cel?
- De evolutie van slijm:hoe komen we aan al dit slijm?
- Welke organel regelt wat binnenkomt en verlaat de kern?
- Groepen cellen zijn georganiseerd in wat?
- Nieuw model voorspelt veranderingen in hout

- Een uitvinding maakt de productie van een natuurlijke zoetstof mogelijk
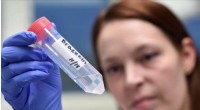
- Chemici slagen erin aminoalcoholen te synthetiseren door gebruik te maken van licht
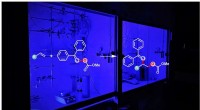
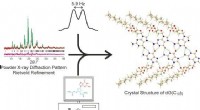
- Nieuwe experimentele strategie verheldert complexe kristalstructuur
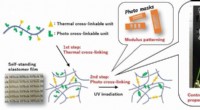
- Films ontwikkelen met instelbare rek en breuk voor verschillende toepassingen
 Wanneer een vallend object de grond raakt, past een opwaartse kracht toe?
Wanneer een vallend object de grond raakt, past een opwaartse kracht toe?  Biomimetische fotodetector ziet in kleur
Biomimetische fotodetector ziet in kleur Pay-per-gaze? Google-patent stelt advertentiesysteem voor
Pay-per-gaze? Google-patent stelt advertentiesysteem voor  Tropische ziekte in middeleeuws Europa herziet de geschiedenis van een ziekteverwekker die verband houdt met syfilis
Tropische ziekte in middeleeuws Europa herziet de geschiedenis van een ziekteverwekker die verband houdt met syfilis Hoe fundamentele natuurkunde en scheikunde de cellulaire functies in primitieve moderne cellen beperken
Hoe fundamentele natuurkunde en scheikunde de cellulaire functies in primitieve moderne cellen beperken  Nieuw materiaal op basis van nanodeeltjes kan antibiotica in water detecteren
Nieuw materiaal op basis van nanodeeltjes kan antibiotica in water detecteren Welke ziekte die wordt gekenmerkt door de onbeperkte groei van abnormale cellen in of op weefsels lichaam staat bekend als wat?
Welke ziekte die wordt gekenmerkt door de onbeperkte groei van abnormale cellen in of op weefsels lichaam staat bekend als wat?  CHIME-telescoop detecteert meer dan 500 mysterieuze snelle radio-uitbarstingen in het eerste jaar van gebruik
CHIME-telescoop detecteert meer dan 500 mysterieuze snelle radio-uitbarstingen in het eerste jaar van gebruik
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

