
Wetenschap
Inzicht in de pH van waterstofperoxide:factoren en overwegingen
* Concentratie: De pH van de waterstofperoxide-oplossing hangt sterk af van de concentratie. Meer geconcentreerde oplossingen zullen zuurder zijn.
* Ontbinding: Waterstofperoxide valt uiteen in water (H₂O) en zuurstofgas (O₂). Dit ontledingsproces wordt versneld door hitte, licht en onzuiverheden, die de pH kunnen beïnvloeden.
* Onzuiverheden: De pH van waterstofperoxide kan worden beïnvloed door onzuiverheden, zoals zuren of basen, die in de oplossing aanwezig kunnen zijn.
Je kunt daarom geen enkele pH-waarde aan waterstofperoxide toekennen. Om de pH te bepalen, moet u de concentratie weten van de specifieke waterstofperoxide-oplossing waarmee u werkt.
Algemene informatie:
* Verdunde waterstofperoxideoplossingen (3%): Deze zijn doorgaans licht zuur, met een pH rond de 6.
* Geconcentreerde waterstofperoxideoplossingen (30% of hoger): Deze zijn zuurder en kunnen een pH van slechts 2 of 3 hebben.
Belangrijke opmerking: Het is van cruciaal belang om voorzichtig om te gaan met waterstofperoxide, vooral in geconcentreerde vormen, omdat het bijtend kan zijn en huidirritatie kan veroorzaken.
 Chemici bedenken een manier om microplastics te verwijderen met okra
Chemici bedenken een manier om microplastics te verwijderen met okra Wat is biologische katalysator dat eiwit in de natuur?
Wat is biologische katalysator dat eiwit in de natuur?  Hoeveel zuurstofmoleculen worden geproduceerd uit de splitsing van twee water als een evenwichtige vergelijking voor reactie als volgt is 2H2O 2H2 plus O2?
Hoeveel zuurstofmoleculen worden geproduceerd uit de splitsing van twee water als een evenwichtige vergelijking voor reactie als volgt is 2H2O 2H2 plus O2?  Hoe windbelastingen te berekenen uit windsnelheden
Hoe windbelastingen te berekenen uit windsnelheden Stikstofmonoxide zou welke van de volgende formules hebben?
Stikstofmonoxide zou welke van de volgende formules hebben?
 Historische aardbevingen suggereren dat Trans-Mexicaanse vulkanische gordels stille regio's actief zijn
Historische aardbevingen suggereren dat Trans-Mexicaanse vulkanische gordels stille regio's actief zijn Een lange periode van inactiviteit waar organismen ongunstige omgevingscondities overleven?
Een lange periode van inactiviteit waar organismen ongunstige omgevingscondities overleven?  Los Angeles:Hollywood, palmbomen en stedelijke olievelden
Los Angeles:Hollywood, palmbomen en stedelijke olievelden Welke twee waterlichamen verbindt het Panamakanaal?
Welke twee waterlichamen verbindt het Panamakanaal?
Een van de technische wonderen van de wereld, het Panamakanaal, sluit zich aan bij de Atlantische Oceaan met de Stille Oceaan door het land Panama in Midden-Amerika. Het land richtte de Panama Can
 Moeder Natuur loopt wild op het smaragdgroene eiland van China
Moeder Natuur loopt wild op het smaragdgroene eiland van China
Hoofdlijnen
- Welke naam wordt gegeven aan de rigide structuur die buiten plasmamembraan wordt gevonden die bacteriecellen omringt en ondersteunt?
- Enzymamplificatie:inzicht in de cruciale rol ervan in de diagnostiek
- Welke factor maakte de evolutie langzaam voor de eerste twee miljard levensjaren op aarde?
- Wat is de Phlogiston?
- Wat functioneert het zenuwstelsel?
- Wat zijn 3 basiscomponenten om de evolutietheorie?
- Waarom die ophef over nurdles?
- Verdeelt meiose geslachtscellen en lichaamscellen?
- Welk organel beweegt materiaal rond de cel?
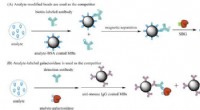
- Nieuwe immunoassaytechniek meet extreem lage concentraties van kleine moleculen met behulp van detectie van één molecuul
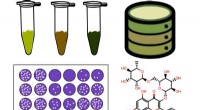
- Een stof in bruinkool kan virussen helpen bestrijden
- Groene waterstof:nanogestructureerd nikkelsilicide schittert als katalysator

- Remedie tegen superbacteriën gevonden in kraaiheide

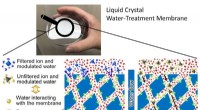
- Zeer selectieve membranen:onderzoekers ontdekken hoe water zijn eigen filtratie kan beïnvloeden
 Onderzoekers werpen licht op hoe ‘microbiële donkere materie’ ziekten kan veroorzaken
Onderzoekers werpen licht op hoe ‘microbiële donkere materie’ ziekten kan veroorzaken  Begrijpen hoe ammoniak de concentratie van hydroxide-ionen verhoogt
Begrijpen hoe ammoniak de concentratie van hydroxide-ionen verhoogt  Wat is de wetenschap van detritivore?
Wat is de wetenschap van detritivore?  Wanneer een elektron van een hoger energieniveau valt naar lager, hoe wordt het vrijgegeven?
Wanneer een elektron van een hoger energieniveau valt naar lager, hoe wordt het vrijgegeven?  Trekt een magnetisch veld elektriciteit aan?
Trekt een magnetisch veld elektriciteit aan?  Wat is een goede superheldennaam voor mobiel?
Wat is een goede superheldennaam voor mobiel?  Welke soort werd het best aangepast aan veranderingen die zich gedurende de langste periode in de omgeving hebben voorgedaan?
Welke soort werd het best aangepast aan veranderingen die zich gedurende de langste periode in de omgeving hebben voorgedaan?  Koeweit gaat tegen 2040 $ 500 miljard uitgeven aan olieprojecten
Koeweit gaat tegen 2040 $ 500 miljard uitgeven aan olieprojecten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

