
Wetenschap
Stoichiometrie:mollen vereist voor zuur-base-neutralisatie (HNO3 en KOH)
Om één mol HNO3 te neutraliseren is één mol KOH nodig. Dit is waarom:
* HNO3 (salpeterzuur) is een sterk monoprotisch zuur. Dit betekent dat het één waterstofion (H+) per molecuul afstaat als het in water wordt opgelost.
* KOH (Kaliumhydroxide) is een sterke monoprotische base. Dit betekent dat het één waterstofion (H+) per molecuul accepteert als het in water wordt opgelost.
De neutralisatiereactie ziet er als volgt uit:
HNO3 (aq) + KOH (aq) → KNO3 (aq) + H2O (l)
In deze reactie:
* Bij één mol HNO3 komt één mol H+-ionen vrij.
* Eén mol KOH accepteert één mol H+-ionen.
Daarom is een molaire verhouding van 1:1 nodig voor volledige neutralisatie.
 De inspanningen van China om de luchtvervuiling in grote steden te verminderen, bleken de vervuiling in nabijgelegen gebieden te vergroten
De inspanningen van China om de luchtvervuiling in grote steden te verminderen, bleken de vervuiling in nabijgelegen gebieden te vergroten Duitsland zou over 10 jaar de laatste gletsjers kunnen verliezen
Duitsland zou over 10 jaar de laatste gletsjers kunnen verliezen Onderzoek naar chemische variaties van carbonaatmineralen om de oliewinning te verbeteren
Onderzoek naar chemische variaties van carbonaatmineralen om de oliewinning te verbeteren Landvormen en waterlichamen in de zuidelijke kolonies
Landvormen en waterlichamen in de zuidelijke kolonies Aanpassing aan de duisternis:hoe gedrags- en genetische veranderingen grotvissen hielpen extreme omgevingen te overleven
Aanpassing aan de duisternis:hoe gedrags- en genetische veranderingen grotvissen hielpen extreme omgevingen te overleven
Hoofdlijnen
- Zijn mannelijke hersenen zo geprogrammeerd dat ze voedsel negeren voor seks?
- Wat betekent orgel in de biologie?
- Kunnen pH van een cel denature -eiwitten?
- Welk type basisbiologisch molecuul absorbeert het lichaam?
- Scheiding komt vaker voor bij albatrosparen met verlegen mannen, studievondsten
- Orka's migreren, studievondsten, maar waarom?
- Belangrijkste verschillen tussen bacterieel chromosomaal DNA en plasmide-DNA
- Hoe reproduceren planten zich als ze zaadloos zijn?
- Wat zijn kenmerken van eukaryoot?
- Microfluïdische chip kan bijwerkingen van radiotherapie verminderen
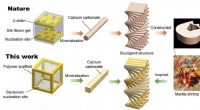
- Kunnen bacteriën sterkere auto's maken, vliegtuigen en bepantsering?
- Chemicaliën die malaria genezen, kunnen ook onkruid doden

- Gerecycled beton en CO₂ uit de lucht verwerkt tot nieuw bouwmateriaal

- Nanodiamanten als fotokatalysatoren

 Lichte aanraking houdt grip op delicate nanodeeltjes
Lichte aanraking houdt grip op delicate nanodeeltjes Elektronentransport in grafeen nanoribbons begrijpen
Elektronentransport in grafeen nanoribbons begrijpen Is pottasiumoxide -zure basic of neutraal oxide?
Is pottasiumoxide -zure basic of neutraal oxide?  Fossiele tandanalyse brengt de vroegste mensen uit zuidelijk Afrika aan het licht
Fossiele tandanalyse brengt de vroegste mensen uit zuidelijk Afrika aan het licht GM voegt snelwegen toe aan semi-autonoom rijsysteem
GM voegt snelwegen toe aan semi-autonoom rijsysteem Waarom is energie belangrijk voor het milieu?
Waarom is energie belangrijk voor het milieu?  NY-regering rapt Amazon-critici te midden van heroverweging van rapporten van bedrijven
NY-regering rapt Amazon-critici te midden van heroverweging van rapporten van bedrijven Wat is een biologisch eiland?
Wat is een biologisch eiland?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

