
Wetenschap
De pH van vitamine C (ascorbinezuur) begrijpen:pKa-waarden uitgelegd
Dit is waarom:
* pKa: De pKa-waarde meet de neiging van een zuur om een proton (H+) af te staan. Het vertelt ons hoe zuur een verbinding is.
* Ascorbinezuur: Ascorbinezuur heeft twee pKa-waarden:
* pKa1 =4,17 :Dit vertegenwoordigt de eerste dissociatie van ascorbinezuur, waarbij het één proton verliest.
* pKa2 =11,57 :Dit vertegenwoordigt de tweede dissociatie, waarbij het een tweede proton verliest.
pH versus pKa:
* pH: De pH van een oplossing vertelt ons hoe zuur of basisch deze is. Het is een maat voor de concentratie H+-ionen in de oplossing.
* pKa: De pKa van een verbinding is een constante waarde die de inherente neiging ervan weerspiegelt om protonen te doneren.
Bepalen van de pH van een ascorbinezuuroplossing:
De pH van een ascorbinezuuroplossing zal afhangen van de concentratie en de aanwezigheid van andere stoffen (bijvoorbeeld buffers). Om de pH te berekenen, moet u rekening houden met beide pKa-waarden en de Henderson-Hasselbalch-vergelijking gebruiken.
Samengevat:
Ascorbinezuur heeft geen enkele pH-waarde. Het heeft twee pKa-waarden, namelijk 4,17 en 11,57. Deze waarden weerspiegelen het vermogen ervan om protonen te doneren en helpen bij het bepalen van de pH van een oplossing die ascorbinezuur bevat.
 Diepzee-ontdekkingsreizigers vinden gezonken oorlogsschip uit belangrijke WO II-strijd
Diepzee-ontdekkingsreizigers vinden gezonken oorlogsschip uit belangrijke WO II-strijd In droge Antarctische valleien, vroege tekenen van door klimaatverandering veroorzaakte verschuivingen in de bodem
In droge Antarctische valleien, vroege tekenen van door klimaatverandering veroorzaakte verschuivingen in de bodem Lijst van dieren in de Arctic
Lijst van dieren in de Arctic Oude parasieten laten zien dat reinheid mogelijk naast ziekte heeft gestaan
Oude parasieten laten zien dat reinheid mogelijk naast ziekte heeft gestaan  Zuid-Afrika heft rampspoed op vanwege droogte
Zuid-Afrika heft rampspoed op vanwege droogte
Hoofdlijnen
- Cellulaire aanpassing:de rol van stress begrijpen
- Heeft de kern iets nodig om goed te functioneren?
- Wat zit er in een naam? Big Data onthult onderscheidende patronen in hogeronderwijssystemen
- Waar bevinden zich lipiden in het lichaam?
- Vul de blanco A in een celgedeelte dat alleen planten kern of celwand hebben die het?
- Hoe verbinden aanpassingen met evolutie?
- Waarom onderzoekers geïnteresseerd zijn in het gezond houden van (sommige) koraalduivels
- Welke volgende kenmerken kunnen worden gebruikt om een organisme in een taxonomisch domein te classificeren?
- Wat is de waarneembare expressie van aanwezige genen en organismen?
- Een elektronensnelweg op weg naar methanol

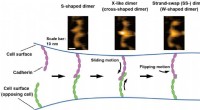
- Visualisatie van bindingsprocessen van cel-celadhesiemoleculen in oplossing
- Onderzoekers evalueren het potentieel van perovskiet-zonnecellen voor ruimtetoepassingen

- Kunstmatige cellen-in-cellen die door licht worden geactiveerd, fungeren als mini-chemische reactoren

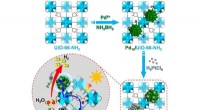
- Legering met één atoom:uitstekende cokatalysator voor fotokatalyse
 Wat is Inconel?
Wat is Inconel?  OLYMPUS-experiment werpt licht op de structuur van protonen
OLYMPUS-experiment werpt licht op de structuur van protonen Handsignalen verbeteren het succes van videovergaderingen
Handsignalen verbeteren het succes van videovergaderingen Hoe een hekel aan lessen het vreemdgaan van studenten beïnvloedt
Hoe een hekel aan lessen het vreemdgaan van studenten beïnvloedt Wat is orthodoxe fysica?
Wat is orthodoxe fysica?  Voor welke organismen test Voges-Proskauer?
Voor welke organismen test Voges-Proskauer?  Welke planeet is 93 miljoen mijl verwijderd van de zon?
Welke planeet is 93 miljoen mijl verwijderd van de zon?  Kan deskundig redeneren worden aangeleerd?
Kan deskundig redeneren worden aangeleerd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

