
Wetenschap
Redox-halfreacties:elektronenoverdracht begrijpen
Redox-halfreacties:het verhaal van elektronenoverdracht
Redoxreacties omvatten de overdracht van elektronen tussen chemische soorten. In plaats van naar de hele reactie te kijken, kunnen we deze opsplitsen in twee halve reacties , die elk het oxidatie- of reductieproces vertegenwoordigen dat afzonderlijk plaatsvindt.
1. Oxidatie-halfreactie:
- Deze halfreactie toont het verlies van elektronen per soort.
- De soort die oxidatie ondergaat, wordt het reductiemiddel genoemd (het veroorzaakt reductie bij een andere soort).
- Elektronen verschijnen als producten aan de rechterkant van de vergelijking.
Voorbeeld:
Fe²⁺(aq) → Fe³⁺(aq) + e⁻
(IJzer(II) verliest een elektron en wordt ijzer(III))
2. Reductie-halfreactie:
- Deze halfreactie toont de winst van elektronen per soort.
- De soort die reductie ondergaat, wordt het oxidatiemiddel genoemd (het veroorzaakt oxidatie bij een andere soort).
- Elektronen verschijnen als reactanten aan de linkerkant van de vergelijking.
Voorbeeld:
Cu²⁺(aq) + 2e⁻ → Cu(s)
(Koper(II) krijgt twee elektronen om massief koper te worden)
Belangrijkste punten:
- Balanceren: Beide halfreacties moeten in termen van atomen en lading in evenwicht zijn. Vaak wordt hierbij water (H₂O), waterstofionen (H⁺) of hydroxide-ionen (OH⁻) toegevoegd, afhankelijk van de omgeving van de reactie (zuur, basisch of neutraal).
- Combineren: De twee halfreacties kunnen worden gecombineerd om de algehele gebalanceerde redoxreactie te vormen. Dit omvat het aanpassen van coëfficiënten om ervoor te zorgen dat het aantal elektronen dat verloren gaat bij oxidatie gelijk is aan het aantal elektronen dat wordt gewonnen bij reductie.
Waarom zijn halfreacties nuttig?
- Complexe reacties vereenvoudigen: Ze maken het gemakkelijker om het elektronenoverdrachtsproces te begrijpen.
- Haalbaarheid van reacties voorspellen: Ze helpen bepalen of een reactie spontaan zal optreden of niet.
- Elektrochemische cellen begrijpen: Ze zijn essentieel voor het beschrijven van de werking van batterijen en brandstofcellen.
Voorbeeld van het combineren van halfreacties:
Laten we de oxidatie- en reductiehalfreacties uit de bovenstaande voorbeelden combineren:
Oxidatie: Fe²⁺(aq) → Fe³⁺(aq) + e⁻
Reductie: Cu²⁺(aq) + 2e⁻ → Cu(s)
Om ze te combineren:
1. Vermenigvuldig de oxidatiehalfreactie met 2 om de elektronen in evenwicht te brengen:2Fe²⁺(aq) → 2Fe³⁺(aq) + 2e⁻
2. Tel de twee halfreacties bij elkaar op:2Fe²⁺(aq) + Cu²⁺(aq) + 2e⁻ → 2Fe³⁺(aq) + Cu(s) + 2e⁻
3. Annuleer de elektronen:2Fe²⁺(aq) + Cu²⁺(aq) → 2Fe³⁺(aq) + Cu(s)
Dit is de algehele evenwichtige redoxreactie.
Het begrijpen van redox-halfreacties is cruciaal voor het begrijpen en analyseren van een breed scala aan chemische processen. Door redoxreacties op te splitsen in deze eenvoudiger stappen, krijgen we waardevolle inzichten in hun mechanismen en potentiële toepassingen.
Hoofdlijnen
- Nieuwe aanwijzingen waarom mutaties in het MYH9-gen een breed spectrum aan aandoeningen bij mensen veroorzaken
- Hoe kan een polaire geneeskunde zich anders in uw lichaam gedragen dan niet -polair?
- Wat is weefsel in een levend organisme?
- Wetenschappers tonen respect voor sommige parasieten
- Waarom is een elektronenmicroscoop bijzonder nuttig geweest en bacteriën bestudeerd?
- Bloedcelvorming:waar en hoe hematopoëse optreedt
- Wat is een necleotide?
- Inzicht in slapheid:oorzaken en biologische betekenis
- Is een blaarkever een omnivoor?
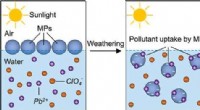
- Onderzoekers onderzoeken milieuverwering van microplastics, opname van verontreinigende stoffen
- Hoe u de zuiverheid van stoffen kunt verifiëren:van visuele controles tot geavanceerde spectroscopie

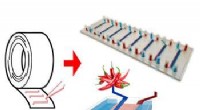
- Met gewone tape, onderzoekers maken chip die de ontwikkeling van medicijnen kan versnellen
- Nieuw elektrodemateriaal ontwikkeld om de laadcapaciteit van lithiumbatterijen te vergroten
- Goedkoop, efficiënte en stabiele foto-elektrode kan de watersplitsing met zonne-energie verbeteren

 Hoe gebruiken planten water in fotosynthese?
Hoe gebruiken planten water in fotosynthese?  Wat is waar aan eendimensionale beweging?
Wat is waar aan eendimensionale beweging?  Het ontrafelen van het wanneer, waar en hoe van vulkaanuitbarstingen
Het ontrafelen van het wanneer, waar en hoe van vulkaanuitbarstingen Heeft de maan Triton een magnetisch veld?
Heeft de maan Triton een magnetisch veld?  Wat is de relatie tussen richting van een elektrisch veld en kracht die zou uitoefenen?
Wat is de relatie tussen richting van een elektrisch veld en kracht die zou uitoefenen?  Wat zijn cellen die zich niet kunnen voortplanten?
Wat zijn cellen die zich niet kunnen voortplanten?  Wat moet er worden toegepast om elektronen in dezelfde richting te laten bewegen?
Wat moet er worden toegepast om elektronen in dezelfde richting te laten bewegen?  Kan de maan tegelijkertijd ondergaan dat de zon opkomt?
Kan de maan tegelijkertijd ondergaan dat de zon opkomt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


