
Wetenschap
Methyloranje-titratie:mechanisme in de zuur-base-chemie (Na2CO3 en HCl)
1. De chemie van methyloranje
* Methyloranje is een zwak zuur dat in twee vormen voorkomt:
* Zuurvorm (HIn): Rode kleur
* Basisformulier (In-): Gele kleur
* Het evenwicht tussen deze vormen wordt beschreven door de volgende vergelijking:
HIn (rood) ⇌ H+ + In- (geel)
* De positie van dit evenwicht wordt beïnvloed door de pH van de oplossing.
2. Titratieproces
* Initiële status: Bij aanvang van de titratie bevat de oplossing natriumcarbonaat (Na2CO3), een zwakke base. Hierdoor ontstaat een enigszins basale omgeving. Methyloranje is een zwak zuur en bevindt zich meestal in de basevorm (In-), wat resulteert in een geel oplossing.
* Als HCl wordt toegevoegd: Als u zoutzuur (HCl) toevoegt, reageert het met het natriumcarbonaat. Bij deze reactie worden hydroxide-ionen (OH-) verbruikt, waardoor het evenwicht naar de zure kant verschuift. Dit zorgt ervoor dat meer methyloranje overgaat van de basevorm (In-) naar de zure vorm (HIn).
* Equivalentiepunt: Het equivalentiepunt wordt bereikt wanneer het aantal toegevoegde mol HCl gelijk is aan het aanwezige aantal mol Na2CO3. Op dit punt bestaat de oplossing voornamelijk uit het zwakke zuur H2CO3 (koolzuur). De pH van de oplossing ligt rond 4,5, wat het eerste equivalentiepunt van de titratie is.
* Eindpunt: Het eindpunt van de titratie vindt plaats wanneer de indicator van kleur verandert. In dit geval verandert de methyloranje van geel in oranje (een mengsel van rood en geel). Deze kleurverandering vindt plaats wanneer de pH van de oplossing het pH-bereik van methyloranje (3,1-4,4) bereikt.
* Tweede gelijkwaardigheidspunt: Verdere toevoeging van HCl leidt tot het tweede equivalentiepunt waar alle carbonaationen worden geneutraliseerd. Op dit punt bestaat de oplossing voornamelijk uit het zwakke zuur H2CO3 en de geconjugeerde base HCO3-. De pH van de oplossing ligt rond 8,3.
3. Waarom methyloranje geschikt is
Methyloranje is een geschikte indicator voor deze titratie omdat:
* Duidelijke kleurverandering: De kleurverandering van geel naar oranje is duidelijk en gemakkelijk zichtbaar.
* pH-bereik: Het pH-bereik van methyloranje (3,1-4,4) overlapt met het eerste equivalentiepunt van de titratie (pH ~ 4,5). Dit zorgt ervoor dat de indicator van kleur verandert dichtbij het punt waar alle Na2CO3 heeft gereageerd met HCl.
Samengevat: De kleurverandering van methyloranje tijdens de titratie van natriumcarbonaat met zoutzuur weerspiegelt de verschuiving in de pH wanneer het sterke zuur de zwakke base neutraliseert. De kleurverandering signaleert het eindpunt van de titratie, dat dicht bij het eerste equivalentiepunt van de reactie ligt.
 Landbouw wordt riskanter onder klimaatverandering
Landbouw wordt riskanter onder klimaatverandering Lachgas heeft misschien geholpen om de vroege aarde te verwarmen en leven te geven
Lachgas heeft misschien geholpen om de vroege aarde te verwarmen en leven te geven Onderzoeksproject voor Grade 5
Onderzoeksproject voor Grade 5  De bossen in Ghana worden weggevaagd:wat zit hierachter en waarom pogingen om dit tegen te houden niet werken?
De bossen in Ghana worden weggevaagd:wat zit hierachter en waarom pogingen om dit tegen te houden niet werken?  Hoe helpt wetenschap ons te weten over de wereld?
Hoe helpt wetenschap ons te weten over de wereld?
Hoofdlijnen
- Welke activiteit zou de coördinatie van beide hersenen van de hemisferen vereisen?
- Verspreiden bacteriën en virus zich op dezelfde manier?
- Hoe een smalspectrumantibioticum zich richt op C. difficile
- Komen soorten samen of divergeren ze naarmate ze evolueren?
- Wat zijn de 2 gordels van het menselijk lichaam?
- Vergelijk en contrasteer het zenuwstelsel met endocrien systeem?
- Waar komen de gameten vandaan in de levenscyclus van een plant?
- Eiwitsynthese:hoe mRNA en aminozuren eiwitten in het ribosoom assembleren
- Wat is een goede superheldennaam voor mobiel?
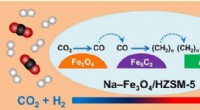
- Wetenschappers ontwikkelen efficiënte multifunctionele katalysator voor CO2-hydrogenering tot benzine
- Nieuwe technologie zet afvalplastic in een uur om in vliegtuigbrandstof

- Oorsprong van het leven:chemische evolutie in een kleine Golfstroom

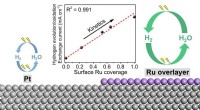
- Nieuwe mechanismen voor verbetering van de activiteit van bimetaalkatalysatoren voor waterstofopwekking en brandstofcellen
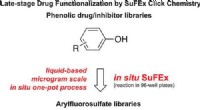
- Click-chemiereacties kunnen de potentie van kankerbestrijdende medicijnen versterken
 Vraagtekens bij het verband tussen vervuiling door magnetietdeeltjes en de ziekte van Alzheimer
Vraagtekens bij het verband tussen vervuiling door magnetietdeeltjes en de ziekte van Alzheimer Hubble onderzoekt de archeologie van de oude hub van onze Melkweg
Hubble onderzoekt de archeologie van de oude hub van onze Melkweg Wat zijn manometrische vloeistoffen?
Wat zijn manometrische vloeistoffen?  10 zwarte wetenschappers die je moet kennen
10 zwarte wetenschappers die je moet kennen  Wetenschappers ontdekken hoe planten grote wortelziekten bestrijden
Wetenschappers ontdekken hoe planten grote wortelziekten bestrijden  Wat zou er gebeuren als zonne -energie opraakt?
Wat zou er gebeuren als zonne -energie opraakt?  Welk molecuul is de gemakkelijke vorm van energie die door cellen wordt gebruikt?
Welk molecuul is de gemakkelijke vorm van energie die door cellen wordt gebruikt?  Welk apparaat converteert warmte -energie om te werken?
Welk apparaat converteert warmte -energie om te werken?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

