
Wetenschap
Ionische verbindingen een naam geven:een stapsgewijze handleiding
1. Eerst kation, daarna anion
* Katie: Het positief geladen ion (metaal).
* Anion: Het negatief geladen ion (niet-metaal).
2. Gebruik de namen van het element
* De naam van het kation blijft hetzelfde.
* De naam van het anion krijgt een achtervoegselwijziging:
* -ide: Voor de meeste niet-metalen vervangt u de uitgang door "-ide".
* Voorbeeld:Chloor wordt chloride.
* -ite: Voor polyatomaire ionen die eindigen op "-ite"
* Voorbeeld:Sulfiet blijft sulfiet.
* -at: Voor polyatomaire ionen die eindigen op "-ate"
* Voorbeeld:Sulfaat blijft sulfaat.
3. Speciale gevallen behandelen
* Overgangsmetalen: Sommige overgangsmetalen vormen meerdere ionen. Gebruik Romeinse cijfers om hun lading aan te geven.
* Voorbeeld:FeCl₂ is ijzer(II)chloride omdat Fe een lading van +2 heeft.
* Polyatomische ionen: Deze ionen zijn groepen atomen met een totale lading. Je moet hun namen en aanklachten kennen.
* Voorbeeld:Na₂SO₄ is natriumsulfaat (sulfaat is een polyatomisch ion).
Voorbeelden:
* NaCl:natriumchloride
* MgO:Magnesiumoxide
* Al₂O₃:aluminiumoxide
* CuCl₂:Koper(II)chloride
* NH₄Cl:Ammoniumchloride
Belangrijkste punten
* Schrijf altijd eerst het kation en daarna het anion.
* De namen van de elementen worden gebruikt, waarbij de naam van het anion wordt gewijzigd.
* Vergeet niet om Romeinse cijfers te gebruiken voor overgangsmetalen met meerdere mogelijke ladingen.
* Polyatomaire ionen zijn groepen atomen met een totale lading.
* U kunt een periodiek systeem gebruiken om metalen en niet-metalen en hun typische ladingen te identificeren.
 Wat is het atoomnummer van COOH?
Wat is het atoomnummer van COOH?  Medische instrumenten worden gesteriliseerd onder de heetst mogelijke temperaturen, leg uit waarom ze in een autoclaaf een apparaat zijn dat in wezen snoepkoker en verwarmt Inst?
Medische instrumenten worden gesteriliseerd onder de heetst mogelijke temperaturen, leg uit waarom ze in een autoclaaf een apparaat zijn dat in wezen snoepkoker en verwarmt Inst?  Mol koolmonoxide (CO) berekenen - een stapsgewijze handleiding
Mol koolmonoxide (CO) berekenen - een stapsgewijze handleiding  De vorming van een gas als gevolg van de ontsnapping met hoge energie-deeltjes Surface Liquid staat bekend als?
De vorming van een gas als gevolg van de ontsnapping met hoge energie-deeltjes Surface Liquid staat bekend als?  Wat creëert zuurstof gemengd met chloor?
Wat creëert zuurstof gemengd met chloor?
 Digitale tools voor het behoud van bosdiversiteit
Digitale tools voor het behoud van bosdiversiteit Groen van woede:vrouwelijke leiders in klimaatverandering worden geconfronteerd met online aanvallen
Groen van woede:vrouwelijke leiders in klimaatverandering worden geconfronteerd met online aanvallen Waarom is de onze een eindige aarde?
Waarom is de onze een eindige aarde?  Speelde de aurora borealis een rol bij het tot zinken brengen van de Titanic?
Speelde de aurora borealis een rol bij het tot zinken brengen van de Titanic? Welk niveau bezetten mensen op een ecologische piramide?
Welk niveau bezetten mensen op een ecologische piramide?
Hoofdlijnen
- Wat zijn twee levende delen van een ecosysteem?
- Class You MHC -genencode voor?
- Welke van deze is een infectieus eiwitviroïde virusprion?
- Waarom zijn membraaneiwitten nodig voor actief transport?
- Wat zijn het twee verschillende soort endoplasmatisch reticulum doen?
- Waarom is het essentieel dat levende exemplaren worden waargenomen?
- Wat is belangrijk voor de evolutie van de theorie voor de moderne biologie?
- Wat draagt de informatie om een proteoom te produceren?
- Wat is een symbiotische relaties Wat betekent elk?
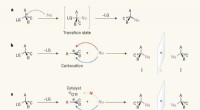
- Een SN1-reactie gebruiken om quaternaire stereocentra te maken
- Een goede kop koffie zetten is afhankelijk van scheikunde en natuurkunde

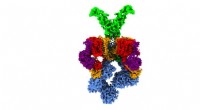
- Wetenschappers lossen 3D-structuur van nanomachine op die tuberculose virulent maakt
- Nieuwe methoden voorgesteld om polymere lamellaire kristallen te karakteriseren

- Filmtechnologie inspireert draagbare vloeistofeenheid die energie wil oogsten

 Wat zijn de meest voorkomende mineralen van de boom?
Wat zijn de meest voorkomende mineralen van de boom?  Heeft de afstand tot de zon invloed op hoe lang per jaar op die planeet is?
Heeft de afstand tot de zon invloed op hoe lang per jaar op die planeet is?  Welke lijn is dichter bij de evenaar 30n of 15s?
Welke lijn is dichter bij de evenaar 30n of 15s?  Wat helpt calciumcarbonaat en aluminiumhydroxide neutraliseren?
Wat helpt calciumcarbonaat en aluminiumhydroxide neutraliseren?  Het superzware zwarte gat in ons sterrenstelsel onderzoeken
Het superzware zwarte gat in ons sterrenstelsel onderzoeken Hoeveel ounces zijn gelijk aan 210 gram?
Hoeveel ounces zijn gelijk aan 210 gram?  Wat voor soort energie zit in de producten van fotosynthese?
Wat voor soort energie zit in de producten van fotosynthese?  Hoe bouw je een succesvolle eierdruppelcontainer voor natuurkunde
Hoe bouw je een succesvolle eierdruppelcontainer voor natuurkunde
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

