
Wetenschap
Trigonale vlakke moleculen en ionen:identificatie en voorbeelden
Trigonale vlakke geometrie begrijpen
* Centraal Atoom: Het centrale atoom in een trigonaal vlak molecuul heeft drie bindingsparen van elektronen en geen alleenstaande paren.
* Bondhoeken: De bindingshoeken tussen de drie atomen gebonden aan het centrale atoom zijn ongeveer 120°.
* Vorm: De drie atomen gebonden aan het centrale atoom vormen een platte driehoek, met het centrale atoom in het midden.
Voorbeelden van trigonale vlakke moleculen en ionen:
* Boortrifluoride (BF₃): Borium heeft drie valentie-elektronen en vormt drie enkele bindingen met fluoratomen. Dit resulteert in een trigonale vlakke structuur.
* Kooldioxide (CO₂): Koolstof heeft vier valentie-elektronen en vormt twee dubbele bindingen met zuurstofatomen. Voor het bepalen van de vorm worden de dubbele bindingen behandeld als enkele bindingen. CO₂ heeft dus een trigonale vlakke structuur.
* Nitraation (NO₃⁻): Stikstof heeft vijf valentie-elektronen. Het vormt drie enkele bindingen met zuurstofatomen en heeft één eenzaam elektronenpaar. Het enige paar is echter gedelokaliseerd, wat betekent dat het verspreid is over de drie zuurstofatomen, en dat het de algehele vorm niet significant beïnvloedt. Het nitraation heeft een trigonale vlakke structuur.
* Fosfine (PH₃): Fosfor heeft vijf valentie-elektronen. Het vormt drie enkele bindingen met waterstofatomen en heeft één eenzaam elektronenpaar. Dit eenzame paar duwt de drie waterstofatomen naar beneden, wat resulteert in een trigonale piramidale structuur, en niet trigonaal vlak.
Belangrijkste afhaalmaaltijden:
Om te bepalen of een molecuul of ion een trigonale vlakke vorm heeft, zoekt u naar een centraal atoom met drie bindingsparen en geen alleenstaande elektronenparen.
 Hoe verandert deze blauwe bloementhee van kleur?
Hoe verandert deze blauwe bloementhee van kleur?  Wat 2 door producten van de Krebs -cyclus compleet een cyle begonnen fotosynthese?
Wat 2 door producten van de Krebs -cyclus compleet een cyle begonnen fotosynthese?  Wat is de formule voor kobaltoxide?
Wat is de formule voor kobaltoxide?  Een chaperonine-eiwit, GroEL, heeft een complexer mechanisme dan eerder werd gedacht
Een chaperonine-eiwit, GroEL, heeft een complexer mechanisme dan eerder werd gedacht Elementair boor wordt geproduceerd in een industrieel proces door het verwarmen van Diboron-trioxide W magnesiummetaal ook oxide produceert als bijproduct Hoe schrijf ik onevenwichtige vergelijking voor deze proces?
Elementair boor wordt geproduceerd in een industrieel proces door het verwarmen van Diboron-trioxide W magnesiummetaal ook oxide produceert als bijproduct Hoe schrijf ik onevenwichtige vergelijking voor deze proces?
Hoofdlijnen
- Kun je organen zien met een microscoop?
- Is een producent een organisme dat andere organismen eet?
- Wat zijn enkele van de gemeenschappelijke organismen die in graslandbiomen worden gevonden?
- Welke klier heeft meer exocrien dan endocrien weefsel?
- Wat zijn de twee manieren van reproductie?
- Welke van de volgende is een productcellulaire ademhaling en geen gisting?
- Twee organellen waarvan wordt aangenomen dat ze afstammelingen zijn van eencellige bacteriën zijn?
- Ja,
- Waarom zijn mutaties schadelijk voor het organisme waarin ze plaatsvinden?
- Glas verwerken als een polymeer

- Nieuwe machine learning-techniek analyseert snel nanomedicijnen voor immunotherapie bij kanker
- Professionele gids voor het thermisch behandelen van staal voor optimale hardheid

- Stabiliserende zilverfilms voor zeer efficiënte brandstofcellen

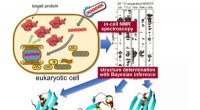
- In-situ meting van 3D-eiwitstructuur in levende eukaryote cellen
 Welke huishoudelijke objecten zijn materie?
Welke huishoudelijke objecten zijn materie?  NASA's Mars 2020 gaat de testkamer binnen
NASA's Mars 2020 gaat de testkamer binnen De aibo-robothond van Sony kan zitten, apporteren en leren wat zijn baasje leuk vindt
De aibo-robothond van Sony kan zitten, apporteren en leren wat zijn baasje leuk vindt  Hoe ver van de korst naar de kern?
Hoe ver van de korst naar de kern?  Dit is waarom studenten niet herzien wat ze schrijven - en waarom ze dat zouden moeten doen
Dit is waarom studenten niet herzien wat ze schrijven - en waarom ze dat zouden moeten doen Misvattingen in de diepzee veroorzaken onderschatting van de effecten van mijnbouw op de zeebodem
Misvattingen in de diepzee veroorzaken onderschatting van de effecten van mijnbouw op de zeebodem Waarom wordt er zo weinig energie doorgegeven?
Waarom wordt er zo weinig energie doorgegeven?  Heeft een zwart gat-etende ster neutrino's gegenereerd? Onwaarschijnlijk, zo blijkt uit nieuw onderzoek
Heeft een zwart gat-etende ster neutrino's gegenereerd? Onwaarschijnlijk, zo blijkt uit nieuw onderzoek
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

