
Wetenschap
Elektronegativiteitsrangschikking:zwavel, zuurstof, neon, aluminium - uitgelegd
Elektronegativiteit begrijpen
Elektronegativiteit is de maatstaf voor het vermogen van een atoom om elektronen aan te trekken in een chemische binding. Hoe hoger de elektronegativiteit, hoe sterker de aantrekkingskracht.
Trends in elektronegativiteit
* Stijgt over een periode (van links naar rechts): Atomen in dezelfde periode hebben hetzelfde aantal elektronenschillen, maar naarmate je door de periode beweegt, neemt het aantal protonen in de kern toe. Deze sterkere positieve lading trekt de elektronen dichterbij, waardoor ze moeilijker te verwijderen zijn.
* Verkleint per groep (van boven naar beneden): Naarmate je een groep lager gaat, worden de elektronenschillen groter. De buitenste elektronen bevinden zich verder van de kern en de aantrekkingskracht is zwakker.
De elementen rangschikken
1. Neon (Ne): Neon is een edelgas, wat betekent dat het een volledige buitenste schil van elektronen heeft. Het heeft een zeer lage elektronegativiteit omdat het geen elektronen meer hoeft op te nemen.
2. Aluminium (Al): Aluminium is een metaal en metalen hebben doorgaans een lagere elektronegativiteit dan niet-metalen. Het bevindt zich in Groep 13, dus de elektronegativiteit ervan is relatief laag.
3. Zwavel (S): Zwavel is een niet-metaal en niet-metalen hebben over het algemeen een hogere elektronegativiteit dan metalen. Het bevindt zich in groep 16, wat betekent dat het een sterkere aantrekkingskracht op elektronen heeft dan aluminium.
4. Zuurstof (O): Zuurstof is ook een niet-metaal en zit in groep 16. Het bevindt zich echter hoger in de groep dan zwavel, waardoor het elektronegatiever is.
Eindrangschikking (verhogen van de elektronegativiteit)
1. Neon (Ne)
2. Aluminium (Al)
3. Zwavel (S)
4. Zuurstof (O)
 Waterdiefstal een groeiend probleem in het steeds droger wordende Spanje
Waterdiefstal een groeiend probleem in het steeds droger wordende Spanje Na een kernoorlog, 's werelds noodvoedselvoorziening zou zeevruchten kunnen zijn - als overbevissing nu stopt
Na een kernoorlog, 's werelds noodvoedselvoorziening zou zeevruchten kunnen zijn - als overbevissing nu stopt Noem 5 producenten in een ecosysteem?
Noem 5 producenten in een ecosysteem?  Wat beschreef de wetenschappers het beste die hebben bijgedragen aan de huidige hoeveelheid kennis?
Wat beschreef de wetenschappers het beste die hebben bijgedragen aan de huidige hoeveelheid kennis?  Duurzame start-ups moeten eerst corporate venture capital overwegen
Duurzame start-ups moeten eerst corporate venture capital overwegen
Hoofdlijnen
- In welk biome leven de apen?
- Wat omdat mensen hun eigen voedsel niet kunnen produceren en moeten eten welk organisme zijn ze?
- Wat zijn condensatie -kernen?
- Door alles te proberen, leert de roofzuchtige zeeslak wat hij niet mag eten
- Waar vindt het ATP-PCR-systeem plaats in cel?
- Wat zijn tweehuizige en monocious planten?
- Welke gespecialiseerde cellen zijn verantwoordelijk voor het overbrengen van berichten in het hele lichaam?
- Veel fylogenetische bomen zijn gebaseerd op DNA -sequentie -overeenkomsten Wat is het praktische resultaat van deze gelijkenis?
- Geef voorbeelden van hoe systeembiologie van invloed kan zijn op de medische praktijk of het maken van milieubeleid?
- Gladde vloeistofoppervlakken verwarren mosselen

- Door in een rockster-materiaal te knijpen, kan het stabiel genoeg worden voor zonnecellen

- Algen als microscopisch kleine bioraffinaderijen
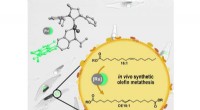
- Gebruik van nabij-infrarood licht om een oor in het lichaam in 3D te printen

- Hoe een functionele moleculaire machine te coderen?
 Digitale tools voor het behoud van bosdiversiteit
Digitale tools voor het behoud van bosdiversiteit Luchtvaartmaatschappijen nemen geen risico met onze veiligheid - en kunstmatige intelligentie ook niet
Luchtvaartmaatschappijen nemen geen risico met onze veiligheid - en kunstmatige intelligentie ook niet Hoe beïnvloedt een isolator de stroom van elektriciteit?
Hoe beïnvloedt een isolator de stroom van elektriciteit?  Kunnen geluidsgolven energie doorgeven door lege ruimte?
Kunnen geluidsgolven energie doorgeven door lege ruimte?  Afvalmelk kan worden gebruikt om de uitstoot van kooldioxide in elektriciteitscentrales te verminderen
Afvalmelk kan worden gebruikt om de uitstoot van kooldioxide in elektriciteitscentrales te verminderen Studie plaagt voorkeur voor positief nieuws
Studie plaagt voorkeur voor positief nieuws Science Projects on Kinematics
Science Projects on Kinematics Waar bevindt zich de vulkaanriem?
Waar bevindt zich de vulkaanriem?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

