
Wetenschap
Natriumion (Na+) versus neonatoom (Ne):belangrijkste verschillen verklaard
1. Aantal elektronen:
* Natriumion (Na+): Heeft 10 elektronen. Het verliest één elektron uit zijn neutrale toestand om positief geladen te worden.
* Neonatoom (Ne): Heeft 10 elektronen. Het is van nature een neutraal atoom, wat betekent dat het hetzelfde aantal protonen en elektronen heeft.
2. Opladen:
* Natriumion (Na+): Heeft een lading van +1 omdat hij een elektron heeft verloren.
* Neonatoom (Ne): Heeft een neutrale lading (0).
3. Elektronenconfiguratie:
* Natriumion (Na+): 1s² 2s² 2p⁶ (hetzelfde als neon)
* Neonatoom (Ne): 1s² 2s² 2p⁶
4. Chemische reactiviteit:
* Natriumion (Na+): Is relatief niet-reactief vanwege zijn stabiele elektronenconfiguratie.
* Neonatoom (Ne): Is zeer onreactief (een edelgas) vanwege zijn volledige buitenste elektronenschil.
In wezen heeft een natriumion dezelfde elektronenconfiguratie als een neonatoom, waardoor het zeer stabiel is. Dit is de reden waarom natrium gemakkelijk zijn buitenste elektron verliest en een positief ion vormt.
Belangrijkste afhaalmaaltijden: Natriumionen en neonatomen vertonen verschillend chemisch gedrag, ondanks dat ze hetzelfde aantal elektronen en dezelfde elektronenconfiguratie hebben. Dit verschil komt voort uit het feit dat het natriumion een positieve lading draagt, terwijl het neonatoom neutraal is.
Hoofdlijnen
- Heterotrofen zijn organismen die wat kunnen?
- Hoe poliepen van de maankwallen virale aanvallen op hun microbioom afweren
- Wat gaat er in en uit de cel?
- Hoe gebruiken wetenschappers genetisch bewijs bij het classificeren van organismen?
- Welke categorie bevat de meeste organismen?
- Moleculaire modellen:hoe ze zich verhouden tot andere modellen
- De meeste cellen in het menselijk lichaam zijn.
- Wat is de naam van subeenheidstructuur -eiwitten?
- Wat zou er gebeuren als een pathogeen van een enkele cel kweekgerecht zou betreden?
- Wetenschappers maken waterfiltratiemembranen die zichzelf kunnen reinigen

- Vetzuurgrondstoffen zorgen voor een zeer efficiënte glyoxylaat‐TCA-cyclus voor een hoogproductieve productie van β‐alanine

- Hoe de polariteit van water het leven vormgeeft:van oplosbaarheid tot plantentransport

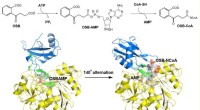
- Wetenschappers onthullen verschillende substraatbindingsmodus in o-succinylbenzoyl-CoA-synthetase
- Saptechniek kan de gezondheid van vers geperst sap beïnvloeden

 Waarom is vrouwelijke seksualiteit flexibeler dan mannelijke seksualiteit?
Waarom is vrouwelijke seksualiteit flexibeler dan mannelijke seksualiteit?  Lineaire versneller voor energieterugwinning voorgesteld voor natuurkundig onderzoek van de volgende generatie
Lineaire versneller voor energieterugwinning voorgesteld voor natuurkundig onderzoek van de volgende generatie Wat is het eerste land bewoond door mensen?
Wat is het eerste land bewoond door mensen?  Welke laag van de atmosfeer ontvangt voldoende energie van zon om moleculen en atomen uit elkaar te breken?
Welke laag van de atmosfeer ontvangt voldoende energie van zon om moleculen en atomen uit elkaar te breken?  Vijf verschillende soorten fossielen
Vijf verschillende soorten fossielen  Kun je de lithium -ionbatterij 3.7V 1100 mAh naar je mobiele telefoon LG 1000mAh gebruiken?
Kun je de lithium -ionbatterij 3.7V 1100 mAh naar je mobiele telefoon LG 1000mAh gebruiken?  Is leeftijd gekoppeld aan het beeld van de perfecte partner?
Is leeftijd gekoppeld aan het beeld van de perfecte partner?  Kustecosystemen wereldwijd:koolstofreservoirs van miljarden dollars
Kustecosystemen wereldwijd:koolstofreservoirs van miljarden dollars
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


