
Wetenschap
Tariefwet uitgelegd:hoe de concentratie van reactanten de reactiesnelheid beïnvloedt
Tarievenwet:
```
Tarief =k[A]^m[B]^n
```
waar:
* Beoordeel: De snelheid van de reactie, doorgaans gemeten in eenheden van M/s (mol per liter per seconde).
* k: De snelheidsconstante, een evenredigheidsconstante die de intrinsieke snelheid van de reactie weerspiegelt.
* [A] en [B] zijn respectievelijk de concentraties van reactanten A en B.
* m en n zijn de volgorden van de reactie met betrekking tot respectievelijk reactanten A en B. Het zijn exponenten die experimenteel zijn bepaald en die aangeven hoe de snelheid verandert met de concentratie van elke reactant.
Uitleg:
* De snelheidswet stelt dat de snelheid van een reactie direct evenredig is met het product van de concentraties van de reactanten tot hun respectievelijke ordes.
* De volgorde van de reactie met betrekking tot een specifieke reactant wordt experimenteel bepaald.
* Als de bestelling 0 is , de snelheid is onafhankelijk van de concentratie van die reactant.
* Als de bestelling 1 is , is de snelheid direct evenredig met de concentratie van die reactant.
* Als de bestelling 2 is , is de snelheid evenredig met het kwadraat van de concentratie van die reactant.
* De algemene volgorde van de reactie is de som van de individuele orders met betrekking tot elke reactant (in dit geval m + n).
Voorbeeld:
Beschouw de reactie:
```
A + 2B → C
```
Als de experimenteel bepaalde snelheidswet is:
```
Tarief =k[A]^1[B]^2
```
dan:
* De reactie is van de eerste orde met betrekking tot A (m =1).
* De reactie is van de tweede orde ten opzichte van B (n =2).
* De algemene volgorde van de reactie is 3 (m + n =1 + 2).
Dit betekent dat een verdubbeling van de concentratie van A de snelheid zal verdubbelen, terwijl een verdubbeling van de concentratie van B de snelheid zal verviervoudigen.
 Welk element heeft 6 koolstofatomen 12 waterstof- en zuurstofatomen?
Welk element heeft 6 koolstofatomen 12 waterstof- en zuurstofatomen?  Is de reactie tussen waterstof en zuurstof een combinatiereactie?
Is de reactie tussen waterstof en zuurstof een combinatiereactie?  Wat betekent het als we zeggen dat een stof in water oplosbaar is?
Wat betekent het als we zeggen dat een stof in water oplosbaar is?  Wat gebeurt er met chemische bindingen wanneer nieuwe verbindingen worden gevormd in een reactie?
Wat gebeurt er met chemische bindingen wanneer nieuwe verbindingen worden gevormd in een reactie?  Welke bijdragen heeft J.J. Thomson Make to the Atom?
Welke bijdragen heeft J.J. Thomson Make to the Atom?
Hoofdlijnen
- Wat zijn de belangrijkste functie van agar in plantenweefselcultuurmedium?
- Onderzoekers beschrijven hoe sperma de weg kwijt kan raken
- Hoe cellen fouten corrigeren onder tijdsdruk
- Wat is de naam van kleverige witte dingen in een cel?
- Wat vraagt een prokaryotische cel om replicatie te stoppen en verdeeldheid te ondergaan?
- Welke opkomende feiten over mariene biologie?
- Wat zijn enkele voorbeelden van kern?
- Phineas Gage:het ongeluk dat de moderne neurowetenschappen lanceerde
- Wat doet een Physichiater?
- Kalium-aangedreven oplaadbare batterijen:een poging tot een duurzamer milieu

- Sensoren voor de versheid van voedsel kunnen de houdbaarheidsdatum vervangen om voedselverspilling tegen te gaan
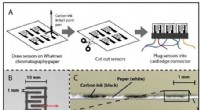
- Laserstraalexcitatie heeft geen invloed op de nucleofiele substitutiereactie

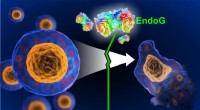
- Biochemici ontdekken een enzym om celdood te stoppen
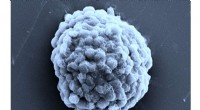
- Onderzoek creëert waterstofproducerende levende druppeltjes, weg vrijmaken voor alternatieve toekomstige energiebron
 Als twee objecten van verschillende temperaturen in contact zijn, is de overdrachtsenergie ertussen een vorm aan die wordt genoemd?
Als twee objecten van verschillende temperaturen in contact zijn, is de overdrachtsenergie ertussen een vorm aan die wordt genoemd?  Het proces dat verantwoordelijk is voor de enorme energie in de zon is?
Het proces dat verantwoordelijk is voor de enorme energie in de zon is?  Kubieke voeten converteren naar Lbs
Kubieke voeten converteren naar Lbs  De eigenschappen van een nieuwe klasse brillen voorspellen
De eigenschappen van een nieuwe klasse brillen voorspellen Wat zijn de drie domeinen van menselijk handelen?
Wat zijn de drie domeinen van menselijk handelen?  Hoeveel principes van het tillen van het dragen en verplaatsen van zware objecten zijn er?
Hoeveel principes van het tillen van het dragen en verplaatsen van zware objecten zijn er?  Hoe ver is de aarde van Mercurey?
Hoe ver is de aarde van Mercurey?  Drones kunnen op een dag honingbijen helpen bestuiven
Drones kunnen op een dag honingbijen helpen bestuiven
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

