
Wetenschap
Loodchloridesynthese:de reactie met natrium en nitraat begrijpen
* Lead is niet betrokken: De reagentia die u heeft genoemd zijn natrium (Na) en nitraat (NO₃⁻). Er is geen lood (Pb) aanwezig.
* Nitraat is een polyatomisch ion: Nitraat (NO₃⁻) is een negatief geladen ion en kan niet op zichzelf bestaan. Het moet worden gecombineerd met een positief geladen ion om een neutrale verbinding te vormen.
* Natriumnitraat is een stabiele verbinding: Natrium en nitraat reageren en vormen natriumnitraat (NaNO₃), een stabiele verbinding.
Om loodchloride (PbCl₂) te maken, moet je een loodverbinding laten reageren met een chlorideverbinding. Bijvoorbeeld:
Reactie:
Lood(II)nitraat (Pb(NO₃)₂) + Natriumchloride (NaCl) → Loodchloride (PbCl₂) + Natriumnitraat (NaNO₃)
Gebalanceerde vergelijking:
Pb(NO₃)₂(aq) + 2NaCl(aq) → PbCl₂(s) + 2NaNO₃(aq)
Uitleg:
* Bij de reactie ontstaat een neerslag van loodchloride (PbCl₂), omdat dit onoplosbaar is in water.
* De coëfficiënten vóór elke verbinding zorgen ervoor dat het aantal atomen van elk element aan beide kanten van de vergelijking gelijk is.
 Onderzoekers gebruiken aminozuren om hoogwaardige dunne koperfilms te laten groeien
Onderzoekers gebruiken aminozuren om hoogwaardige dunne koperfilms te laten groeien Welke 2 dingen gaan in fotosynthese?
Welke 2 dingen gaan in fotosynthese?  Wetenschappers bootsen de dodelijke kaak van een worm na om veerkrachtige materialen te ontwerpen en te vormen
Wetenschappers bootsen de dodelijke kaak van een worm na om veerkrachtige materialen te ontwerpen en te vormen Wat zijn de kenmerken van solide materie?
Wat zijn de kenmerken van solide materie?  Is ureum een verzadigde verbinding?
Is ureum een verzadigde verbinding?
 UM-analyse daagt U.S. Postal Service-milieuonderzoek voor elektrische voertuigen uit
UM-analyse daagt U.S. Postal Service-milieuonderzoek voor elektrische voertuigen uit Wat is de niche van een blad?
Wat is de niche van een blad?  Wat is het verschil tussen een natuurlijk en gecultiveerd bos?
Wat is het verschil tussen een natuurlijk en gecultiveerd bos?  Gemeden door microben, organische koolstof is bestand tegen afbraak in ondergrondse omgevingen
Gemeden door microben, organische koolstof is bestand tegen afbraak in ondergrondse omgevingen Wat zijn enkele bedreigde dieren in de aarde Grasland Biom?
Wat zijn enkele bedreigde dieren in de aarde Grasland Biom?
Hoofdlijnen
- Waarom zouden verschillende enzymen temperatuurbereiken hebben met optimale temperaturen?
- Hoe kan het weten dat plantencellen chloroplasten hebben en dieren u niet helpen de manier waarop planten voedsel krijgen te vergelijken?
- Zijn de vadergenen altijd dominante genen?
- Welke woorden gebruiken bioloog?
- Waar in het lichaam gebeurt ademhaling?
- Hoe worden individuele versies van genen genoemd?
- Welk eten heeft enzym?
- Wat is de functie van teenstructuur op een rotifer?
- Biologen maken kever met functioneel extra oog
- Geneesmiddelgeïnduceerde celmembraancomplexen induceren de dood van kankercellen

- Nieuwe moleculaire val reinigt meer radioactief afval van splijtstofstaven

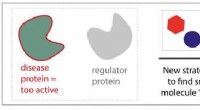
- Hoe moleculaire lijmen te vinden om ziekten effectief aan te pakken?
- Goedkope hernieuwbare energie:het fotosyntheseproces doorbreken dat planten in staat stelt om wat te splitsen

- Hygroscopische polymere gels:het verzamelen van zoet water en energie uit luchtvochtigheid
 Welke laag van een bodemprofiel vormt eerst uit de basis?
Welke laag van een bodemprofiel vormt eerst uit de basis?  Welke moleculen bepalen de weefselspecificiteit van hormonen?
Welke moleculen bepalen de weefselspecificiteit van hormonen?  Een stuk rots of metaal uit de ruimte dat de atmosfeer van de aarde binnenkomt met hoge snelheid en brandt op?
Een stuk rots of metaal uit de ruimte dat de atmosfeer van de aarde binnenkomt met hoge snelheid en brandt op?  Wat zijn enkele voorbeelden van goede geleiders?
Wat zijn enkele voorbeelden van goede geleiders?  In een vijver zouden de algen en vissen andere levensvormen vormen welke wetenschappers de bevolking noemen?
In een vijver zouden de algen en vissen andere levensvormen vormen welke wetenschappers de bevolking noemen?  Hoeveel chloormoleculen zitten er in 134,5 gram chloor?
Hoeveel chloormoleculen zitten er in 134,5 gram chloor?  Sociale media gebruiken in een vroeg stadium een van de vier factoren die verband houden met hogere verspreidingspercentages van COVID-19
Sociale media gebruiken in een vroeg stadium een van de vier factoren die verband houden met hogere verspreidingspercentages van COVID-19 Hoe is water een kracht?
Hoe is water een kracht?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

