
Wetenschap
Zwakke zuren:de afgifte van waterstofionen in waterige oplossingen begrijpen
Dit is waarom:
* Sterke zuren: Deze zuren ioniseren (breken) volledig in water, waardoor een hoge concentratie H+-ionen vrijkomt. Voorbeelden hiervan zijn zoutzuur (HCl) en zwavelzuur (H2SO4).
* Zwakke zuren: Deze zuren ioniseren slechts gedeeltelijk in water, waardoor een lage concentratie H+-ionen vrijkomt. Ze bestaan in evenwicht met hun niet-geïoniseerde vorm. Voorbeelden hiervan zijn azijnzuur (CH3COOH) en koolzuur (H2CO3).
Belangrijkste kenmerken van zwakke zuren:
* Lage ionisatieconstante (Ka): De Ka-waarde geeft de mate van ionisatie aan. Zwakke zuren hebben een kleine Ka-waarde.
* Lage pH: Hoewel zwakke zuren wel enkele H+-ionen afgeven, hebben ze nog steeds een lagere pH-waarde vergeleken met sterke zuren.
* Evenwicht: Zwakke zuren bestaan in evenwicht met hun geconjugeerde basen. Dit betekent dat ze niet volledig dissociëren in ionen.
Voorbeelden van zwakke zuren:
* Azijnzuur (CH3COOH): Gevonden in azijn.
* Koolzuur (H2CO3): Belangrijk bij het reguleren van de pH van het bloed.
* Citroenzuur (C6H8O7): Gevonden in citrusvruchten.
* Fluorwaterstofzuur (HF): Gebruikt bij het etsen van glas.
Bedenk dat de sterkte van een zuur wordt bepaald door zijn vermogen om H+-ionen in oplossing te doneren. Zwakke zuren doneren minder H+-ionen vergeleken met sterke zuren.
 Geboorte van onderzeese vulkaan voor de oostkust van Afrika tot in detail vastgelegd
Geboorte van onderzeese vulkaan voor de oostkust van Afrika tot in detail vastgelegd Als gevolg van de klimaatverandering kunnen catastrofale bosbranden in Australië elk moment toeslaan
Als gevolg van de klimaatverandering kunnen catastrofale bosbranden in Australië elk moment toeslaan  Video:Aanpak van de effecten van klimaatverandering op de bessenteelt in Europa
Video:Aanpak van de effecten van klimaatverandering op de bessenteelt in Europa Hoe op de natuur gebaseerde oplossingen effectief overstromingsbeheer kunnen bevorderen
Hoe op de natuur gebaseerde oplossingen effectief overstromingsbeheer kunnen bevorderen  Hoe maak je een Dendrogram
Hoe maak je een Dendrogram
Hoofdlijnen
- Wat is een wetenschappelijke theorie en hoe het anders is dan hypothese of wet?
- De delen van een prokaryote identificeren?
- Welke 2 dingen vormen alle celmembranen?
- Wat is het lot van drie kleine cellen die bij oögenese worden geproduceerd?
- Wat zijn beweeglijke processen?
- Wat zijn twee van de dingen die bacteriën nodig hebben om te vermenigvuldigen?
- Waarom is hypothese belangrijk in de wetenschap?
- Waar komt teennagelschimmels vandaan?
- Wanneer de erfenis van een bepaalde eigenschap volgt op patroon welke individuen die heterozygoot zijn voor het hebben van hetzelfde fenotype of fysieke kenmerk als wie homozyg?
- Eiwitten als shuttleservice voor gerichte medicatietoediening

- Chemici maken kunstmatige eiwitten die in het chemische verleden van de aarde kijken

- Hoe water uw lichaamstemperatuur stabiliseert – de wetenschap achter thermoregulatie

- Wetenschappers gebruiken moleculaire kettingen en chemische lichtsabels om platforms te bouwen voor tissue engineering
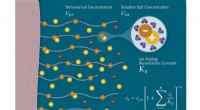
- Onderzoek beschrijft hoe ionen een sleutelrol spelen bij het beheersen van slijmvliesoppervlakken
 Hoe wordt geluidsenergie gedragen?
Hoe wordt geluidsenergie gedragen?  Op welke structuur zijn de stekende cellen van cnidarians gevestigd?
Op welke structuur zijn de stekende cellen van cnidarians gevestigd?  De vluchtige processen die de aarde hebben gevormd
De vluchtige processen die de aarde hebben gevormd Wat is de wetenschappelijke classificatie van ashwagandha?
Wat is de wetenschappelijke classificatie van ashwagandha?  Wat gebeurt er met de frequentie van een eenvoudige slinger wanneer de lengte ervan wordt verdubbeld?
Wat gebeurt er met de frequentie van een eenvoudige slinger wanneer de lengte ervan wordt verdubbeld?  Is recombinatie mapping en genetisch beide betekent hetzelfde?
Is recombinatie mapping en genetisch beide betekent hetzelfde?  Wat gebeurt er als de thermische energie van een materiaal afneemt?
Wat gebeurt er als de thermische energie van een materiaal afneemt?  Tweede huid beschermt tegen chemische, biologische agentia
Tweede huid beschermt tegen chemische, biologische agentia
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

