
Wetenschap
Benzeen:waarom het wordt geclassificeerd als een onverzadigde verbinding | Chemie uitgelegd
1. Waterstoftekort:
* Theoretische verzadiging: Een volledig verzadigde koolwaterstof met zes koolstofatomen zou de formule C6 hebben H14 (volgens de algemene formule Cn H2n+2 ).
* Benzeenformule: Benzeen heeft de formule C6 H6 , wat betekent dat het vier waterstofatomen minder heeft dan een verzadigde verbinding met zes koolstofatomen. Dit ‘waterstoftekort’ is een kenmerk van onverzadiging.
2. Reactiviteit:
* Aanvullingsreacties: In tegenstelling tot verzadigde koolwaterstoffen (alkanen), die relatief niet-reactief zijn, ondergaat benzeen *substitutiereacties*, waarbij een waterstofatoom wordt vervangen door een ander atoom of een andere groep. Dit komt omdat de elektronen in het ringsysteem gedelokaliseerd en stabieler zijn dan een typische dubbele binding.
* Hydrogenatie: Benzeen kan gedwongen worden om hydrogenering te ondergaan, waardoor waterstofatomen aan de ring worden toegevoegd en het gedelokaliseerde systeem wordt verbroken. Dit vereist aanzienlijke energie en druk, wat de onverzadigde aard ervan verder aangeeft.
3. Moleculaire structuur:
* Gedelokaliseerde elektronen: De zes elektronen in de ring zijn niet gelokaliseerd tussen specifieke koolstofatomen, zoals typische dubbele bindingen. In plaats daarvan worden ze gedelokaliseerd en vormen ze een wolk boven en onder het vlak van de ring. Deze delokalisatie draagt bij aan de stabiliteit ervan, maar geeft ook de beschikbaarheid van elektronen voor reacties aan.
4. Spectroscopisch bewijs:
* NMR-spectroscopie: De chemische verschuivingen van de waterstofatomen in benzeen zijn kenmerkend voor een aromatische ring, wat wijst op de delokalisatie van elektronen.
* UV-Vis-spectroscopie: Benzeen absorbeert ultraviolet licht vanwege de gedelokaliseerde pi-elektronen, wat nog een indicatie is van de onverzadigde aard ervan.
Samengevat: Hoewel de structuur van benzeen geen traditionele dubbele bindingen vertoont, bevestigen het waterstoftekort, de reactiviteit, de gedelokaliseerde elektronen en de spectroscopische eigenschappen allemaal dat het een onverzadigde verbinding is. De term "aromatisch" wordt gebruikt om dit unieke type onverzadiging te beschrijven.
 Hoe beïnvloeden oxidatiemiddelen het natuurlijke en kunstmatige kleurpigment?
Hoe beïnvloeden oxidatiemiddelen het natuurlijke en kunstmatige kleurpigment?  Wat is het verschil tussen calciumcarbonaat en bicarbonaat?
Wat is het verschil tussen calciumcarbonaat en bicarbonaat?  Wat is de reactie tussen arseentrioxide en jodium?
Wat is de reactie tussen arseentrioxide en jodium?  Sterke velden en ultrasnelle bewegingen - hoe elektronen in vloeibaar water te genereren en te sturen?
Sterke velden en ultrasnelle bewegingen - hoe elektronen in vloeibaar water te genereren en te sturen? Waarom is thiofeen minder basisch dan furaan?
Waarom is thiofeen minder basisch dan furaan?
 Amerikaans weermodel geüpgraded om extreme gebeurtenissen beter te voorspellen
Amerikaans weermodel geüpgraded om extreme gebeurtenissen beter te voorspellen Een genomische kijk op geobiologie
Een genomische kijk op geobiologie Experts waarschuwen dat klimaatverandering en toenemende bevolking een bedreiging vormen voor de veerkracht van de Britse afvalwaterinfrastructuur
Experts waarschuwen dat klimaatverandering en toenemende bevolking een bedreiging vormen voor de veerkracht van de Britse afvalwaterinfrastructuur Hoe klimaatverandering de aardappelteelt in Zuid-Korea beïnvloedt
Hoe klimaatverandering de aardappelteelt in Zuid-Korea beïnvloedt  Welke natuurlijke fenomenen legt Daedalus en Icarus uit?
Welke natuurlijke fenomenen legt Daedalus en Icarus uit?
Hoofdlijnen
- Wat hebben alle cellen en van enzymen om als biologisch te fungeren?
- Wat doen bioligiest?
- Wat is de belangrijkste functie van een volwassen sporofyt?
- Hoe is een fosfolipide vergelijkbaar met vet?
- Wat is de naam van alle cycli in de wetenschap?
- Wat bevat erfelijke informatie?
- Wat doet ADP in de biologie?
- Hoe een ‘kwal’-vormige structuur de druk in je cellen verlicht
- Maagdelijke vrouwelijke spinnen gevonden bereid om zichzelf over te geven om levend te worden opgegeten door spinnetjes
- Plug-and-play-technologie automatiseert chemische synthese

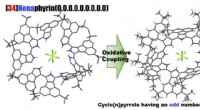
- Synthese van een bijna-infrarood lichtabsorberende macrocyclische aromatische verbinding
- Wetenschappers vinden een verband tussen kanker en veroudering in onze cellen

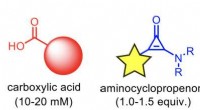
- Door licht geïnduceerde modificatie van een carbonzuur met een aminocyclopropenon
- Hoe werkt gekkotape?

 Welke voedingsmiddelen maken planten?
Welke voedingsmiddelen maken planten?  Gebruikmakend van het grote idee van cellen legt gewoon variatiehulp uit voor wetenschapshuiswerk x?
Gebruikmakend van het grote idee van cellen legt gewoon variatiehulp uit voor wetenschapshuiswerk x?  Voor sommige inheemse stammen in de Zuidelijke Vlaktes is een origineel fluitlied de eerste stap op weg naar een huwelijk
Voor sommige inheemse stammen in de Zuidelijke Vlaktes is een origineel fluitlied de eerste stap op weg naar een huwelijk  Hoe tijd berekenen in decimalen
Hoe tijd berekenen in decimalen Hubble legt zinderende pikzwarte planeet vast
Hubble legt zinderende pikzwarte planeet vast Britse ouders maken zich meer zorgen dat hun kinderen online gepest zullen worden dan die in andere Europese landen, Onderzoek
Britse ouders maken zich meer zorgen dat hun kinderen online gepest zullen worden dan die in andere Europese landen, Onderzoek Spectrale bibliotheek onthult hoe boreale bomen zonnestraling reflecteren
Spectrale bibliotheek onthult hoe boreale bomen zonnestraling reflecteren Uitzicht in de ruimte zijn van het verre verleden?
Uitzicht in de ruimte zijn van het verre verleden?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

