
Wetenschap
Inzicht in de zuur-base-reacties van Arrhenius:definitie en kenmerken
1. Vorming van water: Het belangrijkste kenmerk van een zuur-base-reactie van Arrhenius is de productie van water als product. Dit gebeurt door de reactie van een waterstofion (H+) uit het zuur en een hydroxide-ion (OH-) vanaf de basis.
2. Zuurdefinitie: Een Arrhenius-zuur wordt gedefinieerd als een stof die waterstofionen (H+) doneert wanneer opgelost in water. Voorbeelden hiervan zijn zoutzuur (HCl), zwavelzuur (H2SO4) en salpeterzuur (HNO3).
3. Basisdefinitie: Een Arrhenius-base wordt gedefinieerd als een stof die hydroxide-ionen (OH-) doneert wanneer opgelost in water. Voorbeelden zijn onder meer natriumhydroxide (NaOH), kaliumhydroxide (KOH) en calciumhydroxide (Ca(OH)2).
4. Algemene reactie: De algemene vergelijking voor een zuur-base-reactie van Arrhenius is:
```
Zuur + Base → Zout + Water
```
Voorbeeld:
De reactie tussen zoutzuur (HCl) en natriumhydroxide (NaOH) is een klassiek voorbeeld van een Arrhenius zuur-base-reactie:
```
HCl (aq) + NaOH (aq) → NaCl (aq) + H2O (l)
```
Beperkingen van de Arrhenius-theorie:
Hoewel de Arrhenius-theorie in die tijd baanbrekend was, kent ze beperkingen:
* Het is beperkt tot reacties in water: De theorie verklaart geen reacties in niet-waterige oplosmiddelen.
* Het houdt geen rekening met alle zuren en basen: Er zijn stoffen die kunnen werken als zuren of basen zonder respectievelijk H+ of OH-ionen af te staan.
Bredere theorieën:
De Brønsted-Lowry-theorie en de Lewis-theorie van zuren en basen bieden een uitgebreider begrip van zuur-base-reacties en breiden de definities uit tot buiten het strikte Arrhenius-model.
 Kun je 2 verbindingen scheiden met vergelijkbare retentietijd in een gaschromatografie?
Kun je 2 verbindingen scheiden met vergelijkbare retentietijd in een gaschromatografie?  Wanneer ammoniumcarbonaat ontleedt, wat zou er gebeuren met een gloeiende spalk in aanwezigheid van gassen die worden ontwikkeld?
Wanneer ammoniumcarbonaat ontleedt, wat zou er gebeuren met een gloeiende spalk in aanwezigheid van gassen die worden ontwikkeld?  Wetenschappers ontdekken nieuw veld dat invloed heeft op het stollen van metalen
Wetenschappers ontdekken nieuw veld dat invloed heeft op het stollen van metalen Welke tak van chemie omvat op koolstof gebaseerde moleculen?
Welke tak van chemie omvat op koolstof gebaseerde moleculen?  Waarom worden niet-radioactieve stoffen radioactief wanneer ze in de buurt van een radiumverbinding worden geplaatst?
Waarom worden niet-radioactieve stoffen radioactief wanneer ze in de buurt van een radiumverbinding worden geplaatst?
 Studie onthult wijdverbreid lekrisico voor ondergrondse aardgasopslagputten in de VS
Studie onthult wijdverbreid lekrisico voor ondergrondse aardgasopslagputten in de VS De gevolgen van klimaatverandering projecteren
De gevolgen van klimaatverandering projecteren Aardbevingsvoorspellingen opgegraven in vreemde, gevaarlijk uitgebalanceerde rotsen
Aardbevingsvoorspellingen opgegraven in vreemde, gevaarlijk uitgebalanceerde rotsen 14 algemene bliksemmythen ontkrachten:wat u echt moet weten
14 algemene bliksemmythen ontkrachten:wat u echt moet weten  Kunnen teken eieren bij mensen leggen?
Kunnen teken eieren bij mensen leggen?
Hoofdlijnen
- Gentherapie kan kreupelheid bij paarden genezen, onderzoek vindt
- Wat is de functie van mitose in uw lichaam?
- Wat zijn de elementen afgeleid van de naam van de wetenschapper?
- Wat is de bionaule nomechatuur?
- Wat is de naam voor protisten die hun eigen voedsel kunnen produceren?
- Waar worden eiwitten voor in planten gebruikt?
- Wat classificeert een vraag als wetenschappelijke vraag?
- Welke groep ongewervelde dieren heeft een buisvoet van het watervasculaire systeem?
- Belang van aërobe celbeademing
- Nieuw glow-in-the-dark materiaal kan pad van drugs door het menselijk lichaam volgen

- Onderzoek breekt nieuwe wegen in om te begrijpen hoe een moleculaire motor kracht genereert
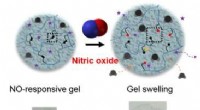
- Wetenschappers ontwikkelen potentieel therapeutische gel, die stikstofmonoxide detecteert, absorbeert overtollig vocht en geeft medicijnen af
- Power-to-gas-installatie met hoog rendement

- Wetenschappers identificeren moleculen die cellen hadden kunnen helpen om te overleven - en te gedijen - op de vroege aarde

 De Poolster is niet de helderste:waarom Sirius echt schijnt
De Poolster is niet de helderste:waarom Sirius echt schijnt  Hoe reist voedselergie van het ene organisme naar het andere?
Hoe reist voedselergie van het ene organisme naar het andere?  Hoe chloor in zwembad verminderen?
Hoe chloor in zwembad verminderen?  Welke technologie is in 1999 uitgevonden?
Welke technologie is in 1999 uitgevonden?  Voordelen en nadelen van het gebruik van wiskundetabellen
Voordelen en nadelen van het gebruik van wiskundetabellen  Waarom gebruikte Hooky de term cellen?
Waarom gebruikte Hooky de term cellen?  Chicago naar Cleveland in 32 minuten? Een hyperloopsysteem zou dat mogelijk kunnen maken. Maar eerst, de technologie moet werken.
Chicago naar Cleveland in 32 minuten? Een hyperloopsysteem zou dat mogelijk kunnen maken. Maar eerst, de technologie moet werken. Een van de twee items die worden gebruikt om stollingsgesteenten te classificeren?
Een van de twee items die worden gebruikt om stollingsgesteenten te classificeren?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

