
Wetenschap
Enkelvoudige vervangingsreacties:gemeenschappelijke omgevingen en sleutelfactoren
Dit is waarom:
* Ionische verbindingen: Bij enkelvoudige vervangingsreacties zijn doorgaans ionische verbindingen betrokken die zijn opgelost in water, waarbij de ionen vrij zijn om te bewegen en op elkaar in te werken.
* Reactiviteitsreeks: De reactiviteit van metalen (of niet-metalen) speelt een cruciale rol. Een reactiever element kan een minder reactief element uit zijn verbinding in oplossing verdringen.
* Elektrochemische processen: De reactie omvat vaak de overdracht van elektronen, waardoor het een elektrochemisch proces wordt.
Voorbeelden:
* Reactie van zink met koper(II)sulfaatoplossing:
```
Zn(s) + CuSO₄(aq) → ZnSO₄(aq) + Cu(s)
```
Hier is zink reactiever dan koper, waardoor het koper uit de oplossing verdringt.
* Reactie van chloorgas met kaliumbromide-oplossing:
```
Cl₂(g) + 2KBr(aq) → 2KCl(aq) + Br₂(l)
```
Chloor is reactiever dan broom en verdringt dus broom uit de oplossing.
Hoewel waterige oplossingen de meest voorkomende omgeving zijn, kunnen enkelvoudige vervangingsreacties ook in andere omgevingen voorkomen, zoals:
* Gesmolten zouten: Er kunnen reacties optreden tussen gesmolten metalen en gesmolten zouten.
* Gasmengsels: Er kunnen reacties optreden tussen reactieve gassen, zoals de reactie van waterstof met chloor om waterstofchloride te vormen.
Waterige oplossingen bieden echter de ideale omstandigheden voor veel enkelvoudige vervangingsreacties vanwege de aanwezigheid van opgeloste ionen en het vermogen om de reacties via elektrochemische processen te laten verlopen.
 Met welke eigenschap van isotopen kan radiotracers nuttig zijn bij het bestuderen van chemische reacties?
Met welke eigenschap van isotopen kan radiotracers nuttig zijn bij het bestuderen van chemische reacties?  Zilvernitrideformule (Ag₃N):inzicht in de chemische samenstelling
Zilvernitrideformule (Ag₃N):inzicht in de chemische samenstelling  Welk gas dient als de uiteindelijke acceptor van elektronen in de?
Welk gas dient als de uiteindelijke acceptor van elektronen in de?  Hoe verschillen elektronen in hetzelfde atoom?
Hoe verschillen elektronen in hetzelfde atoom?  Wat zijn de producten van lichte reacties?
Wat zijn de producten van lichte reacties?
 Wat zijn sommige abiotische factoren in een gematigd regenwoud?
Wat zijn sommige abiotische factoren in een gematigd regenwoud?  De reactie van moessonregens op vulkaanuitbarstingen is afhankelijk van ENSO-staten vóór de uitbarsting
De reactie van moessonregens op vulkaanuitbarstingen is afhankelijk van ENSO-staten vóór de uitbarsting Hoe zullen mensen zich verplaatsen als het klimaat verandert?
Hoe zullen mensen zich verplaatsen als het klimaat verandert? Wat de wereld nu nodig heeft om klimaatverandering te bestrijden:meer moerassen
Wat de wereld nu nodig heeft om klimaatverandering te bestrijden:meer moerassen Satellietgegevens gebruiken om mensen te waarschuwen voor vulkaanuitbarstingen
Satellietgegevens gebruiken om mensen te waarschuwen voor vulkaanuitbarstingen
Hoofdlijnen
- Structuur die het lichaam in 2 delen verdeelt?
- Wat veroorzaakt een breed scala aan fenotypes voor sommige eigenschappen?
- Wat zijn inactieve allelen?
- Hoe zou u het uiterlijk van het DNA -molecuul beschrijven?
- Tot welk orgelsysteem is de thryoïde klier?
- Waarom wordt evolutie als een theorie beschouwd en niet als hypothese of wet?
- Onderzoekers rapporteren bevindingen over de controle van celdeling
- Wat is de studie van biogeologie?
- Het verkennen van een oude gebeurtenis in pompoen, evolutie van kalebas en meloen
- Een venster voor traploos ladingtransport in organische halfgeleiders
- Wanneer chemie met groen licht nabootst wat er in het leven gebeurt

- Onderzoekers bevorderen het begrip van vitaal enzym

- Impact van enzymconcentratie op reactiesnelheden:de relatie begrijpen

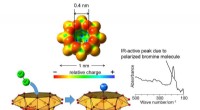
- Polarisatie van broommolecuul in vanadiumoxideclusterholte en nieuwe bromering van alkaan
 Greenpeace voert protest op tegen Poolse boskap
Greenpeace voert protest op tegen Poolse boskap Wat zijn de belangrijkste organismen in de oceaan die fotosynthese uitvoeren?
Wat zijn de belangrijkste organismen in de oceaan die fotosynthese uitvoeren?  Een carbonhydraat bestaande uit twee suikereenheden is een?
Een carbonhydraat bestaande uit twee suikereenheden is een?  Op weg naar een klimaatneutraal Europa:de landsector staat centraal
Op weg naar een klimaatneutraal Europa:de landsector staat centraal Wat is het gebruik van ionisatie?
Wat is het gebruik van ionisatie?  Welk apparaat is bekend wanneer elektronen worden uitgezonden licht schijnt op een metalen oppervlak?
Welk apparaat is bekend wanneer elektronen worden uitgezonden licht schijnt op een metalen oppervlak?  NA2O is geen moleculaire formule waarom?
NA2O is geen moleculaire formule waarom?  Zijn diamanten de beste vriend van GaN? Een revolutie in de transistortechnologie
Zijn diamanten de beste vriend van GaN? Een revolutie in de transistortechnologie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

