
Wetenschap
Koolstofbinding:ionisch versus covalent - Het gedrag van koolstof begrijpen
Dit is waarom:
* Elektronegativiteit: Koolstof heeft een gematigde elektronegativiteit, wat betekent dat het elektronen niet sterk aantrekt en deze ook niet gemakkelijk afgeeft.
* Valentie-elektronen: Koolstof heeft vier valentie-elektronen. Om een stabiel octet te bereiken, is het energetisch gezien gunstiger om deze elektronen te delen met andere atomen door middel van covalente binding, in plaats van elektronen volledig te verliezen of te winnen.
Er zijn echter enkele zeldzame gevallen waarin koolstof ionische verbindingen kan vormen. Dit gebeurt meestal wanneer het reageert met zeer elektropositieve elementen zoals metalen, waarbij carbiden worden gevormd.
Voorbeelden:
* Calciumcarbide (CaC2): In deze verbinding vormt koolstof een C2⁻²-anion met calcium (Ca²⁺)-kation.
Wanneer u 'C' in een chemische formule ziet, duidt dit in de meeste gevallen op een covalente verbinding en niet op een ionische verbinding.
 Wat is de geografie van het bos?
Wat is de geografie van het bos?  Studie onthult enorme diversiteit aan oceaanmicroben
Studie onthult enorme diversiteit aan oceaanmicroben Vulkaanuitbarstingen tijdens massale uitsterving produceerden dezelfde hoeveelheid CO2 als voorspeld wordt uitgestoten in de 21e eeuw
Vulkaanuitbarstingen tijdens massale uitsterving produceerden dezelfde hoeveelheid CO2 als voorspeld wordt uitgestoten in de 21e eeuw Onderzoeksproject over de Atlantische Oceaan benadrukt de wereldwijde inspanningen om de mariene biodiversiteit te behouden
Onderzoeksproject over de Atlantische Oceaan benadrukt de wereldwijde inspanningen om de mariene biodiversiteit te behouden  Inwoners van Noordwest-Indiana, boos over de vervuiling van de raffinaderijen, brengen hun klachten naar een openbare bijeenkomst
Inwoners van Noordwest-Indiana, boos over de vervuiling van de raffinaderijen, brengen hun klachten naar een openbare bijeenkomst
Hoofdlijnen
- Delen van de menselijke hiel
- Wat is een weefsel dat door de plant gaat en voedingsstoffen?
- Is het celmembraan in prokaryotische cel?
- Hoe helpt de structuur van paardenbloemfruit een zaadje om zijn zaden te verspreiden?
- Wat een wetenschappelijke theorie?
- Wat is een niet-voorbeeld van lysosoom?
- Wat in de kern die eigenschappen regelt?
- Wat is de term die wordt gebruikt voor cellen die geen kern hebben?
- Wat zouden de gevolgen van een mutatie die het lichaam verhinderde membraaneiwit te maken dat nodig is voor actief transportsuikerverteringssysteem?
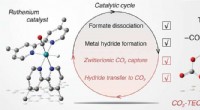
- Monitoring van tussenproducten in CO2-conversie naar formiaat door metaalkatalysator
- De onderbuik van kreeften is net zo sterk als industrieel rubber

- Nieuwe techniek om supersponzen te maken is een game changer

- Glow-in-the-dark papier als sneltest voor infectieziekten

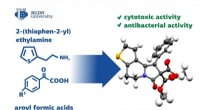
- Chemici ontwikkelen een methode om verbindingen voor geneesmiddelen te synthetiseren
 Waarom bewaart ATP energie voor cellen?
Waarom bewaart ATP energie voor cellen?  Zijn microgolfgolven longitudinaal of transversaal?
Zijn microgolfgolven longitudinaal of transversaal?  Hoe relateer je elektromagnetisch spectrum waar de golven die gewoonlijk licht worden genoemd, vallen op spectrum?
Hoe relateer je elektromagnetisch spectrum waar de golven die gewoonlijk licht worden genoemd, vallen op spectrum?  Waarom hebben mensen geen aardlagen onder de korst gezien?
Waarom hebben mensen geen aardlagen onder de korst gezien?  Wat is de Reeda -schaal?
Wat is de Reeda -schaal?  Wat is de besmetting afgewezen bij omgekeerde osmose?
Wat is de besmetting afgewezen bij omgekeerde osmose?  Fossielen zoals trilobieten die kunnen worden gebruikt om de leeftijd van rotsen op te richten, worden genoemd?
Fossielen zoals trilobieten die kunnen worden gebruikt om de leeftijd van rotsen op te richten, worden genoemd?  Wat gebeurt er als een ster in de loop van de compositie?
Wat gebeurt er als een ster in de loop van de compositie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

