
Wetenschap
Ionische binding uitgelegd:elektronenoverdracht en verschillen met covalente bindingen
Ionische binding omvat de overdracht van een of meer elektronen van het ene atoom naar het andere. Dit is het belangrijkste verschil dat leidt tot de vorming van ionen (atomen met een netto positieve of negatieve lading).
Water (H₂O) is echter geen goed voorbeeld van ionische binding. Water ontstaat door covalente binding waar atomen elektronen delen in plaats van ze over te dragen.
Hier is een overzicht:
* Ionische binding:
* Komt voor tussen metalen (die de neiging hebben elektronen te verliezen) en niet-metalen (die de neiging hebben elektronen te winnen).
*Resulteert in de vorming van ionen met tegengestelde ladingen.
* Voorbeeld:Natriumchloride (NaCl) - Natrium verliest een elektron om een positief ion (Na+) te worden, en chloor krijgt een elektron om een negatief ion (Cl-) te worden. De sterke elektrostatische aantrekkingskracht tussen deze tegengesteld geladen ionen vormt de ionische binding.
* Covalente binding:
* Komt voor tussen niet-metalen.
* Betreft het delen van elektronen tussen atomen.
* Voorbeeld:Water (H₂O) - Elk waterstofatoom deelt een elektron met het zuurstofatoom om een stabiel molecuul te vormen.
Laat het me weten als je nog vragen hebt!
Hoofdlijnen
- Welke gecontroleerde variabelen in de wetenschap?
- Hoe nakomen genen het recessieve nakomelingen?
- Welke hersenstructuur maakt deel uit van het endocriene systeem?
- Wat is celweefsel in plant?
- Welke organel produceert cellulaire energie bij dieren?
- Wat doet een cel in de derde fase van de cyclus?
- Biolife:de betekenis en biologische context begrijpen
- Gistproductie:ethanol, CO2 en meer - een uitgebreide gids
- Zeldzame trofische eieren achter het succes van slangenkopvissen?
- Jelly-uitvinding kan zichzelf genezen als een menselijke huid

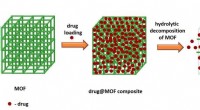
- Voeg gewoon water toe:scheikundigen suggereren een oplossing voor onoplosbare medicijnen
- TNT zou na 116 jaar op pensioen kunnen gaan

- Stof gevonden in fossiele brandstoffen kan veranderen in pure diamant

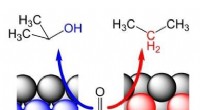
- Omzetting van hernieuwbare grondstoffen op platina vertoont onverwacht gedrag
 Onderzoekers ontdekken bewijs van zes nieuwe fusies van binaire zwarte gaten in LVC-gegevens
Onderzoekers ontdekken bewijs van zes nieuwe fusies van binaire zwarte gaten in LVC-gegevens NASA bekijkt de wolkentemperatuur van orkaan Sergios
NASA bekijkt de wolkentemperatuur van orkaan Sergios Hoeveel gallons is twaalf liter?
Hoeveel gallons is twaalf liter?  Voert gist levensprocessen uit?
Voert gist levensprocessen uit?  New Yorks Central Park wordt officieel autovrij
New Yorks Central Park wordt officieel autovrij Waar komt silicium vandaan?
Waar komt silicium vandaan?  Waarom horen we nucleaire explosies van de zon?
Waarom horen we nucleaire explosies van de zon?  Elektronensnelweg in kristal
Elektronensnelweg in kristal
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


