
Wetenschap
Oplossen van elektrolyten:de ionenvorming in water begrijpen
Dit is waarom:
* Elektrolyten zijn stoffen die elektriciteit geleiden als ze opgelost zijn in water. Dit komt omdat ze dissociëren in geladen deeltjes die ionen worden genoemd.
* Ionen zijn atomen of moleculen die elektronen hebben gewonnen of verloren, waardoor ze een netto positieve of negatieve lading krijgen.
* Wanneer een elektrolyt in water oplost, omringen de watermoleculen de ionen en trekken ze uit elkaar, waardoor de ionische bindingen worden verbroken.
* De resulterende oplossing bevat vrij bewegende ionen, waardoor de oplossing elektriciteit kan geleiden.
Voorbeeld:
Natriumchloride (NaCl) is een elektrolyt. Wanneer het oplost in water, valt het uiteen in natriumionen (Na+) en chloride-ionen (Cl-):
NaCl(s) → Na+(aq) + Cl-(aq)
De "aq" geeft aan dat de ionen zijn opgelost in water (waterige oplossing).
 Wat is de connotatieve betekenis van steen?
Wat is de connotatieve betekenis van steen?  Betere wiskunde levert biljoenen aan klimaatgerelateerde besparingen op:statistici beteugelen de onzekerheid in klimaatmodellen
Betere wiskunde levert biljoenen aan klimaatgerelateerde besparingen op:statistici beteugelen de onzekerheid in klimaatmodellen  Russische onderzoekers onderzoeken grote olieramp in de Zwarte Zee
Russische onderzoekers onderzoeken grote olieramp in de Zwarte Zee Luchtvervuiling keert terug naar pre-COVID-niveaus
Luchtvervuiling keert terug naar pre-COVID-niveaus Studie onderzoekt het vermogen van vrouwen om zich effectief aan te passen aan klimaatverandering
Studie onderzoekt het vermogen van vrouwen om zich effectief aan te passen aan klimaatverandering
Hoofdlijnen
- Wat is het voorbeeld van ongewenste bacteriën?
- Welke organellen zijn talrijker in actieve cellen?
- Wanneer DNA als genen voor het eerst een enkele streng fungeert van wat wordt gemaakt?
- Waar zijn gistchromosomen gevestigd?
- Wat is experimentele groeifunctie?
- Welk niveau van biologische organisatie wordt in alle organismen gevonden?
- Waar staat G 1 in celcyclus voor?
- Wat is de belangrijkste functie van ademhaling in levende organismen?
- Team laat zien hoe de honingbij sommige synthetische pesticiden verdraagt
- Oppervlaktebevochtigbaarheid heeft weinig effect op atmosferische waterverzameling, maar randstructuur is cruciaal

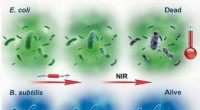
- Selectieve fotothermische therapie met supramoleculaire radicale anionen die in situ worden gegenereerd
- Voorkomen van lithiumverlies voor lithium-ionbatterijen met hoge capaciteit

- Verbinding regelt biologische klok met licht

- De vijfhoek en de boon - de structuur van een eiwit van het immuunsysteem opnieuw tekenen

 Stortplaats omzetten in energie
Stortplaats omzetten in energie Wat is de rol van waterstofbindingen in ijs?
Wat is de rol van waterstofbindingen in ijs?  Video:Wat is witte chocolade?
Video:Wat is witte chocolade?  Hoe de krakeling van zacht naar hard ging - en andere weinig bekende feiten over een van 's werelds favoriete snacks
Hoe de krakeling van zacht naar hard ging - en andere weinig bekende feiten over een van 's werelds favoriete snacks Eenvoudige methode om verontreinigende stoffen in water te binden
Eenvoudige methode om verontreinigende stoffen in water te binden Wat is de definitie van anaërobe systeem?
Wat is de definitie van anaërobe systeem?  Is koolstof een isolator of geleider?
Is koolstof een isolator of geleider?  Een zoektocht naar het beste kan het slechtste in shoppers naar boven halen
Een zoektocht naar het beste kan het slechtste in shoppers naar boven halen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

