
Wetenschap
Natrium versus magnesium:de verschillen in ionisatie-energie begrijpen
Ionisatie-energie begrijpen
Ionisatie-energie is de minimale hoeveelheid energie die nodig is om een elektron te verwijderen uit een gasvormig atoom in zijn elektronische grondtoestand.
Elektronenconfiguratie en afscherming
* Natrium (Na): [Ne] 3s¹
* Magnesium (Mg): [Ne] 3s²
Natrium heeft één elektron in de buitenste schil (3s¹), terwijl magnesium er twee heeft (3s²). Dit eenzame elektron in natrium bevindt zich verder weg van de kern en ervaart een minder effectieve nucleaire lading (de netto positieve lading die een elektron ervaart) vanwege het afschermende effect van de binnenste elektronen.
Effectieve nucleaire lading
De effectieve nucleaire lading is zwakker voor natrium omdat het enkele elektron in de 3s-orbitaal wordt afgeschermd van de kern door de binnenste elektronen (die in de [Ne] kern). In magnesium ervaren de twee 3s-elektronen een sterkere effectieve nucleaire lading omdat ze beide in dezelfde mate worden afgeschermd door de binnenste elektronen.
Belangrijkste punten
* Makkelijker te verwijderen: De zwakkere effectieve nucleaire lading in natrium betekent dat het buitenste elektron minder strak aan de kern is gebonden. Daarom kost het minder energie om dit elektron te verwijderen, wat resulteert in een lagere ionisatie-energie.
* Moeilijker te verwijderen: In magnesium betekent de sterkere effectieve nucleaire lading dat de elektronen steviger aan de kern zijn gebonden, wat leidt tot een hogere ionisatie-energie.
Samengevat: De lagere ionisatie-energie van natrium vergeleken met magnesium is voornamelijk te wijten aan het verschil in effectieve nucleaire lading die de buitenste elektronen ervaren. Het enige buitenste elektron van natrium kan gemakkelijker worden verwijderd omdat het minder aantrekkingskracht op de kern ervaart.
 Wat is de chemische vergelijking voor de reactie van natriumbicarbonaat en ascorbinezuur?
Wat is de chemische vergelijking voor de reactie van natriumbicarbonaat en ascorbinezuur?  Wat is de enkele verplaatsingsreactie van Mg plus H2CO3?
Wat is de enkele verplaatsingsreactie van Mg plus H2CO3?  Een licht schijnen op de vreemde wereld van diwaterstoffosfaatanionen
Een licht schijnen op de vreemde wereld van diwaterstoffosfaatanionen Zijn er drie hydroxide-ionen nodig om een neutrale ionische verbinding te vormen met een aluminiumion?
Zijn er drie hydroxide-ionen nodig om een neutrale ionische verbinding te vormen met een aluminiumion?  Waarom wordt minerale olie toegevoegd aan het flesje dat limwater bevat?
Waarom wordt minerale olie toegevoegd aan het flesje dat limwater bevat?
 Vuur met vuur bestrijden in de Methow Valley
Vuur met vuur bestrijden in de Methow Valley DNA onthult hoe ijstijden Afrikaanse regenwouden beïnvloedden
DNA onthult hoe ijstijden Afrikaanse regenwouden beïnvloedden De afname van de levensduur van bomen in bossen zou een deel van de stijging van de netto koolstofopname kunnen neutraliseren
De afname van de levensduur van bomen in bossen zou een deel van de stijging van de netto koolstofopname kunnen neutraliseren Rederijen kijken naar de toekomst
Rederijen kijken naar de toekomst Weerbureau Macau in onderzoek wegens vertraagde tyfoonwaarschuwing
Weerbureau Macau in onderzoek wegens vertraagde tyfoonwaarschuwing
Hoofdlijnen
- Wat is moleculaire homologie?
- Wat is de functie van een bloemblaadje?
- Sprinkhanenonderzoek zou ons kunnen vertellen waarom Elvis de voorkeur gaf aan boterhammen met pindakaas
- Hoe is genetica gerelateerd aan erfelijkheid?
- Wat voor soort reproductie produceert schimmels die verschillen van beide ouders?
- Wat is het kopiëren van de code en heeft dit betrekking op DNA?
- Hoe de afgelopen 12.000 jaar vorm hebben gegeven aan wat de mens vandaag de dag is
- Welk proces vindt plaats in de kern?
- Waarom zouden wetenschappers een hybride mens-koe-embryo willen creëren?
- Moleculair dunne hybride perovskiet voor geavanceerde opto-elektronische toepassingen

- Biocompatibel binair hologram met mogelijkheden voor medicijnelutie

- Chemici verkrijgen nieuw materiaal voor antibacteriële voedselcoatings
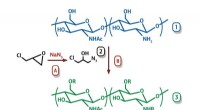
- Dominerende schimmel zou een oplossing kunnen zijn om meer biobrandstoffen en chemicaliën te produceren
- Eiwitten als shuttleservice voor gerichte medicatietoediening

 Het proces door welke bacteriën zich voortplanten?
Het proces door welke bacteriën zich voortplanten?  Indringende vraag:Kun je de handigheid waarmee geboren is veranderen?
Indringende vraag:Kun je de handigheid waarmee geboren is veranderen?  Begrijpen hoe cellen reageren op nanodeeltjes
Begrijpen hoe cellen reageren op nanodeeltjes  NASA gaat drie sondeerraketten lanceren tijdens een zonsverduistering
NASA gaat drie sondeerraketten lanceren tijdens een zonsverduistering  De energieplanten winnen door fotosynthese worden opgeslagen in wat?
De energieplanten winnen door fotosynthese worden opgeslagen in wat?  Onderzoek onthult hoe jagende haviken hun prooi binnen een chaotische zwerm binnendringen
Onderzoek onthult hoe jagende haviken hun prooi binnen een chaotische zwerm binnendringen Hoe geven elektriciteitsleidingen ons elektriciteit?
Hoe geven elektriciteitsleidingen ons elektriciteit?  Waarom meer softwareontwikkeling naar de machines moet gaan
Waarom meer softwareontwikkeling naar de machines moet gaan
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

