
Wetenschap
Picrinezuur:waarom wordt het ondanks zijn eigenschappen een zuur genoemd?
1. Historische naamgeving: Picrinezuur werd voor het eerst ontdekt en benoemd in het begin van de 19e eeuw, voordat ons begrip van chemische binding en zuurgraad zo geavanceerd was. Het werd ‘zuur’ genoemd omdat het zuur was op de manier waarop wetenschappers destijds konden testen:het had een zure smaak, kleurde lakmoespapier rood en reageerde met basen om zouten te vormen.
2. Het is een sterk zuur in water: Hoewel het geen protonen (H+) direct vrijgeeft, lost picrinezuur gemakkelijk op in water en ondergaat het een reactie met watermoleculen. Deze reactie produceert hydroniumionen (H3O+), de eigenlijke zure soorten in oplossing. Hierdoor gedraagt picrinezuur zich als een sterk zuur in waterige oplossingen.
3. Gelijkaardig chemisch gedrag: Ondanks dat het geen echt "protisch zuur" is, deelt picrinezuur veel van dezelfde chemische eigenschappen en reacties als andere sterke zuren. Het vormt zouten met basen, reageert met metalen om waterstofgas te produceren en kan worden gebruikt in verschillende chemische reacties waarbij een sterk zuur vereist is.
4. Algemeen gebruik: De naam "picrinezuur" is zo wijdverbreid gebruikt in de wetenschappelijke gemeenschap dat het moeilijk is om deze te veranderen, ook al hebben we nu een beter begrip van de chemie ervan.
Samengevat: Hoewel picrinezuur technisch gezien niet op dezelfde manier een zuur is als zoutzuur (HCl) of zwavelzuur (H2SO4), hebben de zure eigenschappen ervan in oplossing en het algemene gebruik ervan ertoe geleid dat het een zuur wordt genoemd.
 Wat is het mineraal (Baso4)?
Wat is het mineraal (Baso4)?  Natrium en chloor bevinden zich in dezelfde periode op periodieke tabel Verklaar het verschil in hun afmetingen?
Natrium en chloor bevinden zich in dezelfde periode op periodieke tabel Verklaar het verschil in hun afmetingen?  Waarom boorsulfaat niet bestaat en gerelateerde boorverbindingen
Waarom boorsulfaat niet bestaat en gerelateerde boorverbindingen  Hoeveel mol zijn gelijk aan 3,6 x10 De 23 vermogensmoleculen van zuurstofgas O2?
Hoeveel mol zijn gelijk aan 3,6 x10 De 23 vermogensmoleculen van zuurstofgas O2?  Wat zijn de atomen die make-up Lipiden?
Wat zijn de atomen die make-up Lipiden?
 Tropische storm Ewiniar aanlanding in China gezien door NASA's Aqua-satelliet
Tropische storm Ewiniar aanlanding in China gezien door NASA's Aqua-satelliet Dunner wordende ozonlaag heeft mogelijk 252 miljoen jaar geleden de grootste massa-extinctie op aarde veroorzaakt
Dunner wordende ozonlaag heeft mogelijk 252 miljoen jaar geleden de grootste massa-extinctie op aarde veroorzaakt Onderzoek verlengt lengte van gletsjer- en sneeuwgrensanalyse
Onderzoek verlengt lengte van gletsjer- en sneeuwgrensanalyse Klimaatverandering zal leiden tot abrupte verschuivingen in droge ecosystemen, studie waarschuwt
Klimaatverandering zal leiden tot abrupte verschuivingen in droge ecosystemen, studie waarschuwt Welke soort absorbeert fotonen in een buitenste lagen?
Welke soort absorbeert fotonen in een buitenste lagen?
Hoofdlijnen
- Komt cellen uit reeds bestaan volgens de celtheorie?
- Lichamen die chemicaliën opslaan en vrijgeven voor celgebruik?
- Zebravissen laten zien hoe bio-elektriciteit de spierontwikkeling beïnvloedt
- Hoe leg je de test uit?
- Bacteriën die nitrieten omzetten in nitraten:van bodem tot zee
- Het belangrijkste verschil tussen prokaryotische en eukaryotische cellen is dat?
- Wat is de definitie van intern en extern?
- Plant-dier-interacties:een uitgebreid overzicht
- Als een bioloog zei dat het menselijk lichaam misschien zijn kracht van bacteriën zou halen, zou hij verwijzen naar energiecellen die gebruik maken van in onze darm TRA?
- Eetbare coating voor het bewaren van zeebaars

- Deze kunstmatige eiwitten hebben een stevige greep op metaal
- Nanodeeltjes hebben wat ruimte nodig om energie over te dragen

- Etsproces verbetert de extractie van waterstof tijdens elektrolyse van water
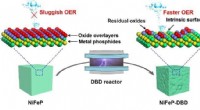
- Chemische processen voorspellen om landbouwbedrijven te helpen, kunstmatig, brandstof- en voedingsindustrie

 Hoe kun je een groot object verplaatsen zonder het aan te raken?
Hoe kun je een groot object verplaatsen zonder het aan te raken?  Nivellering stuitte op wijdverbreide scepsis in heel Engeland, enquêtestudie suggereert:
Nivellering stuitte op wijdverbreide scepsis in heel Engeland, enquêtestudie suggereert: Elektronenkoelkast:ultrasnel koelmechanisme ontdekt in nieuw plasma
Elektronenkoelkast:ultrasnel koelmechanisme ontdekt in nieuw plasma 250 ml is gelijk aan hoeveel liter?
250 ml is gelijk aan hoeveel liter?  PPPL-natuurkundigen essentieel voor nieuwe campagne op 's werelds krachtigste stellarator
PPPL-natuurkundigen essentieel voor nieuwe campagne op 's werelds krachtigste stellarator Wat doet boor in het menselijk lichaam?
Wat doet boor in het menselijk lichaam?  Onderzoeker ziet potentie in het opwekken van energie uit trillingen
Onderzoeker ziet potentie in het opwekken van energie uit trillingen Span van geologische tijd die is onderverdeeld in perioden?
Span van geologische tijd die is onderverdeeld in perioden?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

