
Wetenschap
Factoren die de chemische reactiesnelheid beïnvloeden:een uitgebreide gids
1. Temperatuur: Het verhogen van de temperatuur verhoogt in het algemeen de snelheid van een reactie. Dit komt omdat hogere temperaturen meer kinetische energie aan de reagerende moleculen leveren, wat leidt tot frequentere en krachtigere botsingen die waarschijnlijk zullen resulteren in het verbreken van de binding en de vorming van producten.
2. Concentratie: Een hogere concentratie reactanten leidt doorgaans tot een snellere reactiesnelheid. Dit komt omdat er meer reactantmoleculen aanwezig zijn, waardoor de kans op botsingen en succesvolle reacties groter wordt.
3. Oppervlakte: Voor reacties waarbij vaste stoffen betrokken zijn, zal het vergroten van het oppervlak van de vaste stof in het algemeen de reactiesnelheid verhogen. Dit komt omdat meer van de vaste stof wordt blootgesteld aan de reactanten, waardoor er meer contactpunten en mogelijkheden voor reacties ontstaan. Denk aan een houtblok versus houtkrullen om te verbranden.
4. Katalysator: Een katalysator is een stof die een reactie versnelt zonder daarbij te worden verbruikt. Katalysatoren werken door een alternatieve route voor de reactie te bieden met een lagere activeringsenergie, wat betekent dat de reactie minder energie nodig heeft om te starten.
 Een betere manier om fosfor te beheren?
Een betere manier om fosfor te beheren? Aqua-satelliet ziet tropische depressie Bolaven vechten tegen windschering
Aqua-satelliet ziet tropische depressie Bolaven vechten tegen windschering Hoe beïnvloedt het foerageren van dieren op boomzaden de verdeling en overvloed bomen?
Hoe beïnvloedt het foerageren van dieren op boomzaden de verdeling en overvloed bomen?  Stijgende watertemperaturen brengen de gezondheid van kustecosystemen in gevaar, studie vondsten
Stijgende watertemperaturen brengen de gezondheid van kustecosystemen in gevaar, studie vondsten Overstromingsgegevens van 500 jaar:rivieren en klimaatverandering in Europa
Overstromingsgegevens van 500 jaar:rivieren en klimaatverandering in Europa
Hoofdlijnen
- Menselijk genoomproject:de menselijke DNA-sequentie begrijpen
- Leg de eigenschappen van DNA uit volgens Watson-Crick-model?
- De mens als model voor het begrijpen van biologische fundamenten
- Wat gebeurt er als cellen voedsel afbreken?
- Welke heeft meer cellenplanten of dieren?
- Welke twee stoffen heeft een foetus nodig om volledig potentieel te groeien?
- Waarom zijn alle delen van cellen belangrijk?
- Wat zijn de blauwdrukken in een cel die alle activiteiten regelt?
- Organismen op cellulair niveau kunnen homeostase niet handhaven?
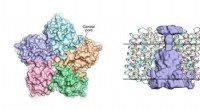
- Wetenschappers onthullen de structuur van virale rodopsines
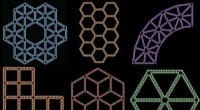
- Computerprogramma kan een 2D-tekening in vrije vorm vertalen naar een DNA-structuur
- Nieuwe tool om polymeereigenschappen te voorspellen

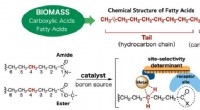
- Een nieuwe tool om chemische complexiteit te creëren uit vetzuren
- Krassen op het oppervlak:metalen implantaten van glas

 Hoe is het weer op Mercurius?
Hoe is het weer op Mercurius?  Studie:Waarom unieke vinken hun hoofden in vele kleuren houden
Studie:Waarom unieke vinken hun hoofden in vele kleuren houden  Hoe wordt stralende energie in een plant gebruikt?
Hoe wordt stralende energie in een plant gebruikt?  De gladheid van ijs uitgelegd
De gladheid van ijs uitgelegd Zou energie beschreven kunnen worden als een kracht of een kracht?
Zou energie beschreven kunnen worden als een kracht of een kracht?  Hoe is energie nuttig?
Hoe is energie nuttig?  Kan goudwinning duurzamer?
Kan goudwinning duurzamer?  Hoe luchthavenbeveiliging werkt
Hoe luchthavenbeveiliging werkt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

