
Wetenschap
Zilverionen en ionische obligaties:het verschil begrijpen
Dit is waarom:
* Ionische bindingen zijn de elektrostatische aantrekkingskrachten tussen tegengesteld geladen ionen. Ze komen *tussen* twee of meer atomen voor.
* Zilverionen zijn enkele, geladen soorten. Ze worden gevormd wanneer een zilveratoom een elektron verliest.
Zie het zo:
* Een ionische binding is als een huwelijk tussen twee ionen.
* Een zilverion is als een alleenstaande persoon, klaar om te trouwen (een ionische band te vormen) met een geschikte partner.
Voorbeelden van ionische bindingen:
* Natriumchloride (NaCl):Natriumionen (Na+) en chloride-ionen (Cl-) worden bij elkaar gehouden door een ionische binding.
* Calciumoxide (CaO):Calciumionen (Ca2+) en oxide-ionen (O2-) worden bij elkaar gehouden door een ionische binding.
Zilverionen kunnen deelnemen aan ionische bindingen. Ze kunnen bijvoorbeeld een ionische binding vormen met een chloride-ion om zilverchloride (AgCl) te creëren. Maar het zilverion zelf is niet de binding; het is een van de deelnemers aan de obligatie.
 Hoe beschrijf je de fysische en chemische eigenschappen die kunnen worden gebruikt om elementen te identificeren?
Hoe beschrijf je de fysische en chemische eigenschappen die kunnen worden gebruikt om elementen te identificeren?  Hoe te berekenen w /v (gewicht per volume)
Hoe te berekenen w /v (gewicht per volume)  Hoe voltooi je de moleculaire vergelijking voor hcl en caco3?
Hoe voltooi je de moleculaire vergelijking voor hcl en caco3?  Hoe kun je ionische verbindingen in een zin gebruiken?
Hoe kun je ionische verbindingen in een zin gebruiken?  Operatie in een pil een mogelijke behandeling voor diabetes
Operatie in een pil een mogelijke behandeling voor diabetes
Hoofdlijnen
- Wilde megalopolis:onderzoek toont onverwachte gebieden met biodiversiteitspeper Los Angeles
- Hoe wetenschappers infectieveroorzakende biofilms bestrijden
- Wat is hetzelfde tussen een celwand en membraan?
- Hoe verschillen de metabole bacteriepaden van eukaryotische cel?
- Hoe wordt de hybride in allel waargenomen?
- Wat zijn enkele voorbeelden van weefsel?
- Waarom is de weefselspecialisatie een voordeel voor meercellige organismen?
- Hoe zijn de rollen van B AN T -cellen vergelijkbaar en verschillend?
- Hormoongevoelige lipase is een enzym dat?
- Onderzoekers tonen aan dat zelfsteriliserende polymeren werken tegen SARS-CoV-2
- NIST gaat met de (slow) flow mee:nieuwe techniek kan biotech verbeteren, precisie geneeskunde

- Legeronderzoek maakt de weg vrij voor nieuwe materialen

- Problemen met bellen vermijden:onderzoek naar de relatie tussen bellen en elektrochemie

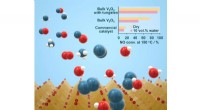
- Door wolfraam vervangen vanadiumoxide ademt frisse lucht in de katalysatortechnologie
 Wat is het percentage samenstelling van elk element dat wordt gevonden in ammoniumsulfide?
Wat is het percentage samenstelling van elk element dat wordt gevonden in ammoniumsulfide?  Welke planeet is 108 miljoen kilometer verwijderd van de zon?
Welke planeet is 108 miljoen kilometer verwijderd van de zon?  Wat is het type stollingsgesteente gevormd onder oppervlakte -aarde?
Wat is het type stollingsgesteente gevormd onder oppervlakte -aarde?  Hoe zijn continenten en tektonische platen gerelateerd?
Hoe zijn continenten en tektonische platen gerelateerd?  Waarom sommige rebellengroepen kinderen dwingen om te vechten:het hangt ervan af hoe ze worden gefinancierd
Waarom sommige rebellengroepen kinderen dwingen om te vechten:het hangt ervan af hoe ze worden gefinancierd Hoe is de energie van een elektron gerelateerd aan niveau IT in?
Hoe is de energie van een elektron gerelateerd aan niveau IT in?  Als het gaat om de levensduur van smartphones, merknaam is belangrijker dan hardware
Als het gaat om de levensduur van smartphones, merknaam is belangrijker dan hardware Een nieuwe methode voor de snelle detectie van een belangrijke antivirale
Een nieuwe methode voor de snelle detectie van een belangrijke antivirale
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

