
Wetenschap
Oxaalzuur versus zwavelzuurtitratie:belangrijkste verschillen verklaard
Hier is een overzicht:
Oxaalzuur (H₂C₂O₄)
* Diprotisch zuur: Oxaalzuur heeft twee zure waterstofatomen . This means it can donate two protons (H⁺) per molecule during titration.
* Titratiecurve: De titratiecurve van oxaalzuur vertoont twee equivalentiepunten , overeenkomend met de neutralisatie van elke zure waterstof. Het eerste equivalentiepunt zal op een lagere pH liggen dan het tweede, omdat het tweede proton minder gemakkelijk wordt gedoneerd.
Zwavelzuur (H₂SO₄)
* Sterk diprotisch zuur: Zwavelzuur is ook een diprotisch zuur , maar het is een sterk zuur . Dit betekent dat het eerste proton in oplossing volledig gedissocieerd is, waardoor het een sterk zuur wordt. Het tweede proton is echter slechts gedeeltelijk gedissocieerd, waardoor het een zwakker zuur wordt.
* Titratiecurve: De titratiecurve voor zwavelzuur toont twee equivalentiepunten , maar het eerste equivalentiepunt zal veel scherper zijn en optreden bij een lagere pH dan het tweede. Dit komt omdat het eerste proton volledig gedissocieerd is en een veel sterker zuur is.
Belangrijkste verschillen tijdens titratie:
* Aantal gelijkwaardigheidspunten: Beide zuren hebben twee equivalentiepunten vanwege hun diprotische aard.
* Equivalentiepunt pH: Het eerste equivalentiepunt voor zwavelzuur zal lager zijn dan het eerste equivalentiepunt voor oxaalzuur vanwege het sterkere eerste proton van zwavelzuur.
* Scherpte van gelijkwaardigheidspunten: Het eerste equivalentiepunt voor zwavelzuur zal scherper zijn dan het eerste equivalentiepunt voor oxaalzuur vanwege de sterk zure aard van het eerste proton.
Samengevat:
Hoewel zowel oxaalzuur als zwavelzuur diprotische zuren zijn, verschilt hun titratiegedrag vanwege de variërende sterkten van hun zure waterstofatomen. De titratiecurve van oxaalzuur zal twee verschillende equivalentiepunten vertonen, terwijl de curve van zwavelzuur een scherper eerste equivalentiepunt zal hebben vanwege de sterk zure aard van het eerste proton.
 De CO2-kosten van thuisbezorging en hoe deze te vermijden
De CO2-kosten van thuisbezorging en hoe deze te vermijden De fundamentele basis van milieuwetenschap als discipline is de?
De fundamentele basis van milieuwetenschap als discipline is de?  Hoe Dyson Spheres werken
Hoe Dyson Spheres werken  Nieuwe studie analyseert vulkanische dodelijke slachtoffers in meer detail dan ooit tevoren
Nieuwe studie analyseert vulkanische dodelijke slachtoffers in meer detail dan ooit tevoren Hoe kunnen wetenschappers voorspellingen vormen over welke omstandigheden het beste zijn voor het kweken van huisplanten?
Hoe kunnen wetenschappers voorspellingen vormen over welke omstandigheden het beste zijn voor het kweken van huisplanten?
Hoofdlijnen
- Kunnen bacteriecellen worden geclassificeerd als plantencellen?
- Welke structuur in de cel is chemische messenger voor DNA?
- Wat biedt instructies aan cellen bij het vormen van orgaan?
- Hoe dragen kunstmatige en natuurlijke selectie bij aan biologische diversiteit?
- Waarom leven sommige planten snel en sterven ze jong?
- Wat is de rol van wetenschap in de samenleving?
- Is een champignon abiotic of een ecosysteem?
- Wat is fertillostion?
- What is another name for Prokaryotic cells that starts with a B?
- Gestructureerde materialen op meerdere schalen voor elektrokatalyse en foto-elektrokatalyse
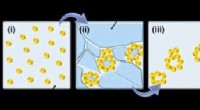
- Artificial Chemist 2.0:Quantum dot R&D in minder dan een uur
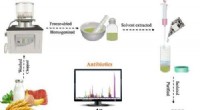
- Sporen van meerdere klassen antibiotica in voedingsmiddelen detecteren
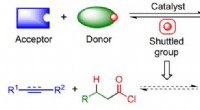
- Voorlopers van zuurchloride maken met behulp van shuttle-katalyse
- Het plaatje van micronutriënten voor plantaardige melkalternatieven compleet

 Hoe zwaartekracht het afzettingsproces beïnvloedt?
Hoe zwaartekracht het afzettingsproces beïnvloedt?  Waar worden kraters van diamanten gevonden?
Waar worden kraters van diamanten gevonden?  NASA wil JOU! om de mensheid voor te bereiden op Mars
NASA wil JOU! om de mensheid voor te bereiden op Mars  Onderzoek:CEO's die minder investeren in maatschappelijk verantwoord ondernemen ondermijnen de veerkracht van hun organisatie
Onderzoek:CEO's die minder investeren in maatschappelijk verantwoord ondernemen ondermijnen de veerkracht van hun organisatie Hoe biokorst bacteriële gemeenschappen in zowel ondergrondse lagen beïnvloedt
Hoe biokorst bacteriële gemeenschappen in zowel ondergrondse lagen beïnvloedt  Wat is de formule voor kwikchloride?
Wat is de formule voor kwikchloride?  Hoe schrijf je de evenwichtige vergelijking tussen een zuur en een basis?
Hoe schrijf je de evenwichtige vergelijking tussen een zuur en een basis?  Onderzoekers kweken regelmatig geordende kristallijne dunne film op nanometerschaal met behulp van poreus 3D-materiaal
Onderzoekers kweken regelmatig geordende kristallijne dunne film op nanometerschaal met behulp van poreus 3D-materiaal
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

