
Wetenschap
Fosforzuur in Redox-titraties:de rol ervan begrijpen
Dit is waarom:
* Redox-titraties omvatten de overdracht van elektronen . Fosforzuur is een zwak zuur en neemt niet gemakkelijk deel aan elektronenoverdrachtsreacties. Het fungeert voornamelijk als protondonor (zuur) en niet als oxidatie- of reductiemiddel.
* Fosforzuur wordt vaak gebruikt bij zuur-base-titraties , waarbij het zijn rol is om een geschikte zure omgeving te bieden waarin de reactie kan plaatsvinden. Het kan ook worden gebruikt om de pH van oplossingen aan te passen.
In plaats van fosforzuur worden bij redoxtitraties doorgaans sterke oxidatie- of reductiemiddelen gebruikt:
* Oxidatiemiddelen: Kaliumpermanganaat (KMnO₄), kaliumdichromaat (K₂Cr₂O₇), cerium(IV)sulfaat (Ce(SO₄)₂)
* Reductiemiddelen: Natriumthiosulfaat (Na₂S₂O₃), ijzer(II)sulfaat (FeSO₄)
Daarom heeft fosforzuur geen specifiek doel bij redoxtitraties. Als u fosforzuur gebruikt bij een titratie, maakt dit waarschijnlijk deel uit van een zuur-base-titratie en niet van een redox-titratie.
 Onderzoekers ontdekken dat klimaatverandering het risico op kwikverontreiniging verhoogt
Onderzoekers ontdekken dat klimaatverandering het risico op kwikverontreiniging verhoogt Wetenschappers vinden ijzersneeuw in de kern van de aarde
Wetenschappers vinden ijzersneeuw in de kern van de aarde Overstromingen treffen meer dan 1 miljoen mensen in Oost-Afrika
Overstromingen treffen meer dan 1 miljoen mensen in Oost-Afrika Het sneeuwdek in Californië is bijna tien jaar hoog. Wat betekent het voor de droogte?
Het sneeuwdek in Californië is bijna tien jaar hoog. Wat betekent het voor de droogte?  Wat kwam de eerste bloeiende planten of zaadplanten?
Wat kwam de eerste bloeiende planten of zaadplanten?
Hoofdlijnen
- Mitose in bloeiende planten is vergelijkbaar met mitosedieren die beide?
- Waar ontwikkelt het menselijke embryo zich?
- Waar in het lichaam gebeurt ademhaling?
- Symbiotische relaties:typen, voorbeelden en belang
- Is Bacillus anthracis prokaryotisch of eukaryotisch?
- Waar bevindt de fotosynthesecel zich?
- Wanneer homologe chromosomen genetische informatie verwisselen als onderdeel van meiose?
- Wat zijn de twee kenmerken van zoogdieren?
- Geen microben? probleem voor rupsen
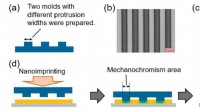
- Onderzoek onthult kwantitatieve en hoge-resolutie drukfuncties van drukgevoelig materiaal
- Middelbare scholieren betrekken bij praktische isotopenactiviteiten

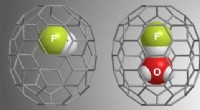
- Onderzoekers isoleren waterstoffluoride en water om zuuroplossing te begrijpen
- Hoe robotwiskunde en smartphones onderzoekers naar een doorbraak in de ontdekking van medicijnen hebben geleid

- Chemici synthetiseren platte siliciumverbindingen

 Welk effect zou een technologie hebben op de wereldeconomie als het nucleaire en hydro -elektriciteit van benzine als energiebron zou vervangen, hoe introduceer ik me aan de gemeenschap?
Welk effect zou een technologie hebben op de wereldeconomie als het nucleaire en hydro -elektriciteit van benzine als energiebron zou vervangen, hoe introduceer ik me aan de gemeenschap?  Een plant heeft een fout in zijn DNA -code voor bepaald eiwit dat het celmembraan vormt, welk effect kan dit op de plant hebben?
Een plant heeft een fout in zijn DNA -code voor bepaald eiwit dat het celmembraan vormt, welk effect kan dit op de plant hebben?  Hoe concurrentie tussen soorten leidde tot een ‘bizar’ patroon in onze eigen evolutionaire stamboom
Hoe concurrentie tussen soorten leidde tot een ‘bizar’ patroon in onze eigen evolutionaire stamboom  Wolkenkrabbers van de toekomst kunnen van hout worden gemaakt
Wolkenkrabbers van de toekomst kunnen van hout worden gemaakt  Waarom zie je ringen van de aarde?
Waarom zie je ringen van de aarde?  Zijn beleefdheidsflushes nuttig – of gezond?
Zijn beleefdheidsflushes nuttig – of gezond?  Hoe de zangvogel zijn melodie leert
Hoe de zangvogel zijn melodie leert  Waarom zien we de zon even nadat hij ondergaat?
Waarom zien we de zon even nadat hij ondergaat?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

