
Wetenschap
Dubbele vervangingsreacties:definitie, voorbeelden en vergelijkingen
Dubbele vervangingsreacties begrijpen
* Definitie: Bij een dubbele vervangingsreactie wisselen de positieve en negatieve ionen van twee reactanten van plaats.
* Algemeen formulier: AB + CD → AD + CB
Voorbeeld
Laten we eens kijken naar de reactie tussen zilvernitraat (AgNO₃) en natriumchloride (NaCl):
* Reactanten:
* Zilvernitraat (AgNO₃):Ag⁺ (zilverion) + NO₃⁻ (nitraation)
* Natriumchloride (NaCl):Na⁺ (natriumion) + Cl⁻ (chloride-ion)
* Producten:
* Zilverchloride (AgCl):Ag⁺ (zilverion) + Cl⁻ (chloride-ion)
* Natriumnitraat (NaNO₃):Na⁺ (natriumion) + NO₃⁻ (nitraation)
Gebalanceerde vergelijking:
AgNO₃(aq) + NaCl(aq) → AgCl(s) + NaNO₃(aq)
Uitleg:
* Het zilverion (Ag⁺) uit zilvernitraat combineert met het chloride-ion (Cl⁻) uit natriumchloride om zilverchloride (AgCl) te vormen.
* Het natriumion (Na⁺) uit natriumchloride combineert met het nitraation (NO₃⁻) uit zilvernitraat en vormt natriumnitraat (NaNO₃).
Belangrijkste kenmerken:
* Twee ionische verbindingen reageren.
* De positieve en negatieve ionen wisselen van partner.
* De reactie vindt meestal plaats in een waterige oplossing (opgelost in water).
* Vaak is één product een neerslag (een vaste stof die uit een oplossing ontstaat). In ons voorbeeld is zilverchloride (AgCl) een neerslag.
Laat het me weten als je meer voorbeelden wilt zien!
 24G CH4 reageert met 96 g O2?
24G CH4 reageert met 96 g O2?  Onderzoekers ontwikkelen injecteerbare biomaterialen op basis van extracellulaire matrix voor herstel van meniscus
Onderzoekers ontwikkelen injecteerbare biomaterialen op basis van extracellulaire matrix voor herstel van meniscus Welk zuur wordt gevormd wanneer de P4O10 reageert met water?
Welk zuur wordt gevormd wanneer de P4O10 reageert met water?  Wetenschappers werpen licht op nieuw goedkoop materiaal om in het donker te zien
Wetenschappers werpen licht op nieuw goedkoop materiaal om in het donker te zien Nieuw ontwikkelde versies van bacteriële enzymen laten zien hoe antibiotica krachtiger zouden kunnen zijn
Nieuw ontwikkelde versies van bacteriële enzymen laten zien hoe antibiotica krachtiger zouden kunnen zijn
 Waarom werpen bomen hun schors af?
Waarom werpen bomen hun schors af?  Bemanningen in Zuid-Spanje worden voor 5e dag geconfronteerd met complexe bosbranden
Bemanningen in Zuid-Spanje worden voor 5e dag geconfronteerd met complexe bosbranden Studie kijkt naar de impact van COVID-19 en cycloon Harold op vissers in Fiji
Studie kijkt naar de impact van COVID-19 en cycloon Harold op vissers in Fiji NASA ziet vorm van Atlantische tropische depressie in het late seizoen
NASA ziet vorm van Atlantische tropische depressie in het late seizoen Winter beperkt innovatie - Een nieuw model voor de biodiversiteit van tropische planten is gebaseerd op het opslageffect
Winter beperkt innovatie - Een nieuw model voor de biodiversiteit van tropische planten is gebaseerd op het opslageffect
Hoofdlijnen
- Welke wetenschappers hebben gewerkt aan de theorie van opkomst?
- Wat is een nucleolus en zijn functie?
- Waar worden organellen gevonden?
- Wat is de wetenschap van het classificeren van organismen in groepen?
- Hoe wordt prokaryotisch DNA genoemd?
- Wat wordt geoxideerd en wat wordt er gereduceerd in celademhaling?
- Wat is een antoniem voor Microbe?
- Zooplankton Vs. fytoplankton
- Een geïntegreerde beoordeling van vaatplantensoorten in Amerika
- De missie van één student om 's werelds meest waardevolle hulpbron te beschermen

- Rekbare zonnecellen een stap dichterbij

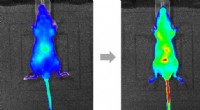
- Vitamine C in het lichaam kan worden gevolgd door fluorescentie
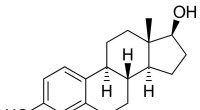
- Oestrogene en anti-oestrogene effecten van PFAS's kunnen afhankelijk zijn van de aanwezigheid van oestrogeen
- Opwindend nieuw materiaal maakt gebruik van zonne-energie om door de mens gemaakte kleurstofverontreinigende stoffen uit water te verwijderen

 Welke structuur is alleen gevonden in een bladcel?
Welke structuur is alleen gevonden in een bladcel?  Is er iets in de naam zinkfosfide dat aangeeft dat er drie en twee fosforionen zijn?
Is er iets in de naam zinkfosfide dat aangeeft dat er drie en twee fosforionen zijn?  Waar haalt magma zijn warmte vandaan en hoe wordt het gehandhaafd?
Waar haalt magma zijn warmte vandaan en hoe wordt het gehandhaafd?  Hoe slim is jouw stad?
Hoe slim is jouw stad? Drie manieren waarop boerderijen van de toekomst de planeet kunnen voeden - en genezen, te
Drie manieren waarop boerderijen van de toekomst de planeet kunnen voeden - en genezen, te Extreme droogte duwt deel van Utahs Great Salt Lake naar laagste niveau
Extreme droogte duwt deel van Utahs Great Salt Lake naar laagste niveau Wat wordt beschouwd als verstoringen in het water veroorzaakt door energie die door water gaat.?
Wat wordt beschouwd als verstoringen in het water veroorzaakt door energie die door water gaat.?  Gouden nanodeeltjes helpen bij eerdere diagnose van leverkanker
Gouden nanodeeltjes helpen bij eerdere diagnose van leverkanker
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

