
Wetenschap
Inzicht in oxidatiegetallen voor overgangsmetalen:een stapsgewijze handleiding
1. Regels om te onthouden:
* Gratis elementen: Het oxidatiegetal van een element in zijn elementaire vorm is altijd 0.
* Monatomische ionen: Het oxidatiegetal van een monoatomair ion is gelijk aan zijn lading. Bijvoorbeeld Fe 2+ heeft een oxidatiegetal van +2.
* Zuurstof: Zuurstof heeft gewoonlijk een oxidatiegetal van -2, behalve in peroxiden (waar het -1 is) en in verbindingen met fluor (waar het positief is).
* Waterstof: Waterstof heeft gewoonlijk een oxidatiegetal van +1, behalve in metaalhydriden waar het -1 is.
* De som van oxidatiegetallen: In een neutrale verbinding moet de som van de oxidatiegetallen van alle atomen gelijk zijn aan nul. In een polyatomair ion moet de som van de oxidatiegetallen gelijk zijn aan de lading van het ion.
2. Strategieën voor transitie-elementen:
* Bekende oxidatietoestanden: Sommige overgangselementen hebben gemeenschappelijke oxidatietoestanden. Bijvoorbeeld
* Chroom heeft vaak +2, +3 en +6 oxidatietoestanden.
* Mangaan heeft gewoonlijk +2, +4, +6 en +7 oxidatietoestanden.
* IJzer is meestal +2 of +3.
* Gebruik de andere elementen: Als je de oxidatiegetallen van de andere elementen in de verbinding kent, kun je het oxidatiegetal van het overgangselement afleiden. Bijvoorbeeld in KMnO4 :
* Kalium (K) heeft een oxidatietoestand van +1.
* Zuurstof (O) heeft een oxidatietoestand van -2.
* Om de ladingen in evenwicht te brengen moet mangaan (Mn) een oxidatietoestand van +7 hebben:(+1) + (+7) + 4(-2) =0
* Anionische liganden: Wanneer overgangselementen complexen vormen met anionische liganden (zoals Cl-, CN-), wordt de oxidatietoestand van het metaal berekend door de totale negatieve lading af te trekken van de totale lading van het complex. Bijvoorbeeld in [Fe(CN)6 ] 4- :
* Cyanide (CN-) heeft een lading van -1.
* De totale kosten van het complex bedragen -4.
* De oxidatietoestand van ijzer (Fe) wordt berekend als +2:-4 - (6 x -1) =+2
3. Voorbeelden:
* FeCl3 : Chloor (Cl) heeft een oxidatiegetal van -1. Om in evenwicht te komen moet ijzer (Fe) een oxidatietoestand van +3 hebben:(+3) + 3(-1) =0
* Cr2 O7 2- : Zuurstof (O) heeft een oxidatiegetal van -2. De totale lading van het dichromaat-ion is -2. Om dit in evenwicht te brengen moet chroom (Cr) een oxidatietoestand van +6 hebben:2(+6) + 7(-2) =-2
* [Co(NH3 )6 ]Cl3 : Ammoniak (NH3 ) is neutraal. Chloride (Cl) heeft een oxidatiegetal van -1. Om dit in evenwicht te brengen moet kobalt (Co) een oxidatietoestand van +3 hebben:(+3) + 3(-1) =0
Belangrijke opmerkingen:
* Variabele oxidatietoestanden: Veel overgangselementen vertonen meerdere oxidatietoestanden, dus het oxidatiegetal kan variëren afhankelijk van de specifieke verbinding.
* Niet altijd gehele waarden: In sommige gevallen is het oxidatiegetal van een overgangselement mogelijk geen geheel getal.
* Formele aanklacht: Oxidatiegetallen zijn een formeel ladingssysteem en vertegenwoordigen niet noodzakelijkerwijs de werkelijke verdeling van elektronen in een molecuul.
Laat het me weten als je specifieke voorbeelden hebt waar je aan wilt werken!
 Zelfvouwende origami:Dankzij chemische programmering kunnen Nafion-vellen worden gevouwen en opnieuw gevouwen
Zelfvouwende origami:Dankzij chemische programmering kunnen Nafion-vellen worden gevouwen en opnieuw gevouwen Wat is warmte- en faseveranderingen?
Wat is warmte- en faseveranderingen?  Wat is de ionische vergelijking voor fosforzuur en bariumhydroxide?
Wat is de ionische vergelijking voor fosforzuur en bariumhydroxide?  Is regen- en elementenmengsel of een compound?
Is regen- en elementenmengsel of een compound?  Waarom verandert methanol van kleur in geel bij toevoeging van natriummetaal?
Waarom verandert methanol van kleur in geel bij toevoeging van natriummetaal?
 De gevolgen voor het klimaat zullen in 2050 het mondiale bbp met bijna een vijfde doen dalen
De gevolgen voor het klimaat zullen in 2050 het mondiale bbp met bijna een vijfde doen dalen  Hoe maak je een Pine-Cone Bird Feeder zonder gebruik van Peanut Butter
Hoe maak je een Pine-Cone Bird Feeder zonder gebruik van Peanut Butter Hernieuwbare energie kan de natuurlijke wereld redden, maar als we niet voorzichtig waren, het zal ook pijn doen
Hernieuwbare energie kan de natuurlijke wereld redden, maar als we niet voorzichtig waren, het zal ook pijn doen Duizenden tonnen microplastics gevonden in Moreton Bay
Duizenden tonnen microplastics gevonden in Moreton Bay  Verontreinigende stoffen veranderen het water in de buurt van Ieodo Island snel
Verontreinigende stoffen veranderen het water in de buurt van Ieodo Island snel
Hoofdlijnen
- Wat is het verschil tussen fysieke en biologische behoeften?
- Welke celorganel heeft een functie van het uitscheidingssysteem?
- Wat betekent hypothese in de wetenschappelijke methode?
- Wat hondeneigenaren moeten weten over leptospirose
- Wat zijn de speciale kenmerken van een pollencel?
- Wat breekt een dubbele DNA-helix uiteen?
- Cellen binnen meercellige organismen zijn gespecialiseerd om specifieke taken uit te voeren. Wat is een voordeel van cellen?
- Hoe een iconische foto van een appel de inspiratie vormde voor een verbeterde celanalyse
- Hoe kunnen prokaryoten succesvoller zijn dan mensen?
- Koffievervalsing ontdekt met nieuwe methode

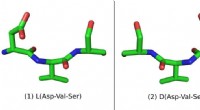
- Door de spiegel:nieuwe spiegelbeeldmoleculen kunnen leiden tot betere medicijnen
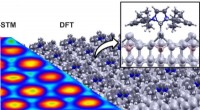
- Nieuwe methode voor de moleculaire functionalisering van oppervlakken
- Nieuwe techniek kan voorheen niet-detecteerbare bacteriën aan het licht brengen op plaatsen waar ze niet gewenst zijn

- Tikken geheimen van Aussie spiders unieke zijde

 Wanneer werd Albert Einstein een beroemde wetenschapper?
Wanneer werd Albert Einstein een beroemde wetenschapper?  Waarom leidt evolutie niet tot perfect aangepaste organismen?
Waarom leidt evolutie niet tot perfect aangepaste organismen?  Hoe Semester Grade te berekenen
Hoe Semester Grade te berekenen  Van wolken tot kraters:Mars Express
Van wolken tot kraters:Mars Express Wat zijn de oorzaken van waterstress?
Wat zijn de oorzaken van waterstress?  Technieken geleerd van de klimaatwetenschap van de aarde helpen bij het zoeken naar mogelijk bewoonbare exoplaneten
Technieken geleerd van de klimaatwetenschap van de aarde helpen bij het zoeken naar mogelijk bewoonbare exoplaneten Nieuw protocol voor organische synthese met organoboorverbindingen en zichtbaar licht
Nieuw protocol voor organische synthese met organoboorverbindingen en zichtbaar licht Een nanotransistor beoordeelt je gezondheid via zweet
Een nanotransistor beoordeelt je gezondheid via zweet
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

