
Wetenschap
Het zuurstofatoom begrijpen:structuur en representatie
1. Het Bohr-model: Dit is een vereenvoudigd model van een atoom. Het toont een centrale kern (die protonen en neutronen bevat) omgeven door elektronen in specifieke energieniveaus die schillen worden genoemd. Voor zuurstof:
* Kern: Bevat 8 protonen en 8 neutronen.
* Elektronen: 2 elektronen in de eerste schil en 6 elektronen in de tweede schil.
2. Lewis-puntstructuur: Dit toont de valentie-elektronen (de elektronen in de buitenste schil) als stippen rond het atoomsymbool. Voor zuurstof:
* Symbool: O
* Punten: ..
O..
3. Kwantummechanisch model: Dit is het meest nauwkeurige model, maar ook het meest complex. Het maakt gebruik van waarschijnlijkheid om te beschrijven waar elektronen waarschijnlijk zullen worden gevonden, in plaats van specifieke banen te tonen. Het wordt weergegeven door complexe vergelijkingen en vormen.
4. 3D-molecuulmodel: Hoewel je een zuurstofatoom niet kunt zien, kun je er wel afbeeldingen van zien in 3D-modellen. Deze modellen tonen de ruimtelijke rangschikking van atomen in een molecuul en kunnen nuttig zijn voor het begrijpen van chemische bindingen en interacties.
Hoe ziet een zuurstofatoom eruit?
Het antwoord hangt af van hoe je het visualiseert. Het is een kleine, complexe structuur die we alleen via modellen kunnen weergeven. Het Bohr-model is een goed startpunt om de basisstructuur te begrijpen, terwijl de Lewis-puntstructuur nuttig is om te begrijpen hoe zuurstof interageert met andere atomen.
 Volgende stap op weg naar een efficiënte biobrandstofcel
Volgende stap op weg naar een efficiënte biobrandstofcel Oorsprong van koper, koolstof en zuurstof:stellaire nucleosynthese
Oorsprong van koper, koolstof en zuurstof:stellaire nucleosynthese  Wat een verschil maakt dagbloem:plant verwijdert giftige koperionen uit verontreinigde grond
Wat een verschil maakt dagbloem:plant verwijdert giftige koperionen uit verontreinigde grond  Kunnen gassen en vloeistoffen warmte transporteren door geleiding?
Kunnen gassen en vloeistoffen warmte transporteren door geleiding?  Hebben alle atomen argon hetzelfde atoomnummer?
Hebben alle atomen argon hetzelfde atoomnummer?
Hoofdlijnen
- Wat is de structuur die eiwitten voorbereidt en verpakt voor gebruik binnen cel of verzending buiten de cel?
- Wat ontdekte Aristoteles in de biologie?
- Hoe wordt een meniscus gebruikt bij het meten?
- Identificeer een orgaan bij mensen dat in staat is tot compenserende hypertrofie?
- Hoe het Curiosity-project werkt
- Wat zijn vier resultaten van wetenschappelijk onderzoek?
- Welke vitamine bevordert de vorming van celmembraan?
- Wat is micro-evolutie?
- Welke twee klassen behoren tot de klasse van stikstofbases die purines worden genoemd?
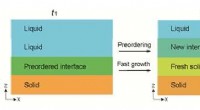
- Domino-achtige kristallisatie van glas
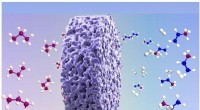
- Wetenschappers persen katalysatoren in gastheermaterialen zoals een schip in een fles

- Poreuze enkelkristallijne monolieten op centimeterschaal met Lewis-zuurplaatsen met hoge dichtheid om propaandehydrogena te verbeteren
- Van flatscreen-tv's tot uw smartphone:het element borium verdient meer aandacht

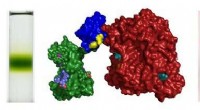
- Team ontwikkelt fotosynthetische eiwitten voor uitgebreide omzetting van zonne-energie
 Wat is de langzaamste chemische reactie?
Wat is de langzaamste chemische reactie?  Hoe wormen de biodiversiteitsexplosie op aarde vormden
Hoe wormen de biodiversiteitsexplosie op aarde vormden  Wat beschrijft de mantel het beste?
Wat beschrijft de mantel het beste?  Kwantum spookachtige actie op afstand wordt praktisch
Kwantum spookachtige actie op afstand wordt praktisch VN-besprekingen over ruimtevredesverdrag bereiken geen consensus
VN-besprekingen over ruimtevredesverdrag bereiken geen consensus Waarom is het regenwoud zo belangrijk voor bewuste mensen?
Waarom is het regenwoud zo belangrijk voor bewuste mensen?  Trofische coherentie verklaart waarom netwerken weinig feedbackloops en een hoge stabiliteit hebben
Trofische coherentie verklaart waarom netwerken weinig feedbackloops en een hoge stabiliteit hebben Cellen vallen in twee brede categorieën, afhankelijk van of ze een celwand hebben?
Cellen vallen in twee brede categorieën, afhankelijk van of ze een celwand hebben?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

