
Wetenschap
Arrhenius-zuren versus Brønsted-Lowry-zuren:het verschil begrijpen
* Arrheniuszuur: Een Arrhenius-zuur is een stof die waterstofionen (H+) produceert wanneer deze in water wordt opgelost.
* Brønsted-Lowry zuur: Een Brønsted-Lowry-zuur is een stof die bij een chemische reactie een proton (H+) afstaat.
* Basis: Een base is een stof die een proton (H+) accepteert.
De bewering "een Arrhenius-zuur is een Brønsted-Lowry-base, geen base" is onjuist.
Dit is waarom:
* Arrhenius-zuren zijn ook Brønsted-Lowry-zuren. De definitie van een Arrhenius-zuur past perfect in de Brønsted-Lowry-definitie. Wanneer een Arrhenius-zuur oplost in water, komen er H+-ionen vrij, die fungeren als protondonoren.
* Arrhenius-zuren zijn geen Brønsted-Lowry-basen. Brønsted-Lowry baseert *accepteert* protonen. Arrheniuszuren *doneren* protonen.
Samengevat:
* Een Arrhenius-zuur is een type Brønsted-Lowry-zuur.
* Arrhenius-zuren voldoen niet aan de definitie van een Brønsted-Lowry-base.
Laat het me weten als je meer uitleg wilt over een van deze definities!
 Een overstromingsexperiment voor kinderen
Een overstromingsexperiment voor kinderen One-hit wonder:hoe prijzen en erkenning de creativiteit van uitvinders verminderen
One-hit wonder:hoe prijzen en erkenning de creativiteit van uitvinders verminderen  Toegenomen smeltende sneeuw in de winter bedreigt westerse watervoorraden
Toegenomen smeltende sneeuw in de winter bedreigt westerse watervoorraden Hoge loodgehaltes in het bloed gevonden bij inheemse volkeren in het Peruaanse Amazonegebied
Hoge loodgehaltes in het bloed gevonden bij inheemse volkeren in het Peruaanse Amazonegebied Waarom zijn Jaguars bedreigde dieren?
Waarom zijn Jaguars bedreigde dieren?
Hoofdlijnen
- Wat is het proces waarin moleculen bewegen en uit de cel bewegen?
- Wat een lijst 20 soorten wetenschap?
- Wat wordt gevormd na ovulatie uit de lege follikel vanwege LH -invloed?
- Onderzoeken hoe microbiomen onze gezondheid beïnvloeden
- Welk systm is belangrijk voor het afbreken van voedsel zodat cellen de voedingen absorberen?
- Hoe fotosynthese licht vangt en het leven op aarde aandrijft
- Wat is de beste manier om cellen te beschrijven?
- Wat is higogeen?
- 5 factoren die leiden tot de vorming van een nieuwe soort?
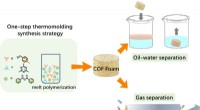
- Gebruik van smeltpolymerisatie om robuust covalent organisch raamwerkschuim te fabriceren
- Belangrijkste eigenschappen van zure stoffen:smaak, pH, reactiviteit en geleidbaarheid

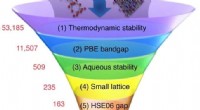
- Uitgebreide elektronische structuurmethoden voor materiaalontwerp
- Lab-on-a-disc-technologie belooft te versnellen, DNA-analyse ter plaatse vereenvoudigen

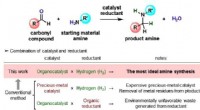
- Het naderen van een ideale aminozuursynthese met behulp van waterstof
 Hoe wordt energie overgedragen via een gemeenschap van organismen?
Hoe wordt energie overgedragen via een gemeenschap van organismen?  Welke tak van wetenschap bestudeert elektriciteit?
Welke tak van wetenschap bestudeert elektriciteit?  Amerikaanse sondefouten Uber, menselijke fout bij zelfrijdende auto-ongeluk
Amerikaanse sondefouten Uber, menselijke fout bij zelfrijdende auto-ongeluk Hoe beschrijft u de chemische reacties die plaatsvinden in verval van voedingsmiddelen?
Hoe beschrijft u de chemische reacties die plaatsvinden in verval van voedingsmiddelen?  Met wat voor soort energie begint de fotosynthese?
Met wat voor soort energie begint de fotosynthese?  Hoeveel mol chloorgas bevindt zich in 9.02x1023 moleculen?
Hoeveel mol chloorgas bevindt zich in 9.02x1023 moleculen?  Zijn er 5 gadgets in welke bimetallische strip wordt gebruikt?
Zijn er 5 gadgets in welke bimetallische strip wordt gebruikt?  Een kan worden voorspeld op basis van zijn locatie in het periodiek systeem?
Een kan worden voorspeld op basis van zijn locatie in het periodiek systeem?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

