
Wetenschap
Begrijpen waarom zuurstof en stikstof gassen zijn bij kamertemperatuur
* Moleculaire structuur: Zowel zuurstof (O2) als stikstof (N2) zijn diatomaire moleculen, wat betekent dat ze bestaan uit twee aan elkaar gebonden atomen. Deze bindingen zijn sterk, maar de krachten tussen individuele moleculen zijn veel zwakker.
* Intermoleculaire krachten: De primaire intermoleculaire krachten die aanwezig zijn in zuurstof en stikstof zijn Londense dispersiekrachten . Dit zijn tijdelijke, zwakke aantrekkingen veroorzaakt door tijdelijke fluctuaties in de elektronenverdeling rond de moleculen.
* Lage kookpunten: Vanwege de zwakke intermoleculaire krachten hebben zuurstof en stikstof zeer lage kookpunten (respectievelijk -183°C en -196°C). Dit betekent dat bij kamertemperatuur de thermische energie van de moleculen voldoende is om de zwakke aantrekkingen te overwinnen, waardoor ze als gas kunnen bestaan.
In tegenstelling daarmee:
* Water (H2O) heeft sterkere intermoleculaire krachten (waterstofbinding) vanwege de polaire aard van het molecuul, waardoor het een veel hoger kookpunt (100°C) heeft.
Samengevat: Zuurstof en stikstof zijn gassen bij kamertemperatuur omdat hun moleculen bij elkaar worden gehouden door zwakke intermoleculaire krachten, wat resulteert in lage kookpunten.
 Noem een product gemaakt met behulp van biologische katalysator?
Noem een product gemaakt met behulp van biologische katalysator?  Veel gemeenschappelijke metalen hebben een specifieke warmte van wat?
Veel gemeenschappelijke metalen hebben een specifieke warmte van wat?  Duurzame plasticvervuiling gemakkelijk, wordt schoon afgebroken met nieuwe katalysator
Duurzame plasticvervuiling gemakkelijk, wordt schoon afgebroken met nieuwe katalysator  Welke stof zou warmteoverdracht door geleiding het beste werken?
Welke stof zou warmteoverdracht door geleiding het beste werken?  Welke apparatuur heb je nodig om moleculen te verbreken?
Welke apparatuur heb je nodig om moleculen te verbreken?
 Een globale kijk op organische koolstof aan de oppervlakte
Een globale kijk op organische koolstof aan de oppervlakte Grotten worden geconfronteerd met nieuwe onbekende na ongekende bosbranden
Grotten worden geconfronteerd met nieuwe onbekende na ongekende bosbranden Klimaatdebat laait op nu uit onderzoek blijkt dat er verschillen zijn tussen voorspellende modellen
Klimaatdebat laait op nu uit onderzoek blijkt dat er verschillen zijn tussen voorspellende modellen Broeikaseffecten op dieren
Broeikaseffecten op dieren Palmolie is overal. Hier is waarom dat ertoe doet.
Palmolie is overal. Hier is waarom dat ertoe doet.
Hoofdlijnen
- Wat zijn prokaryoten?
- Wat gebeurt er met de structuren in kern elke fase profase plus?
- De erfelijke informatie in DNA wordt gecodeerd de volgorde van?
- Is het proces exocytosis materialen die in een cel worden genomen?
- Hoe onderzoekers bacteriën nieuw gedrag leren
- Hoe zorgt de nucleaire envelop toe voor celreproductie?
- Wat zijn de belangrijkste pars van je lichaam?
- Waarom zijn mannelijke spinnen klein, terwijl vrouwtjes gigantisch zijn?
- De buitenste enkele laag van een cel die elkaar overlapt als gordelroos in haar?
- Op de natuur geïnspireerd materiaal maakt gebruik van vloeibare versterking

- De kern van hoe uien je aan het huilen maken
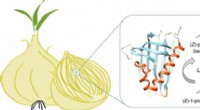
- Studie vindt bewijs voor bestaan van ongrijpbare metabolon
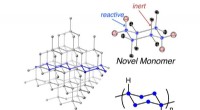
- Nieuw polymeer geïnspireerd op kristallijn silicium om betere computers en zonnecellen te bouwen
- Nooit meer met vuur spelen:onderzoek biedt inzicht in veiligere oplaadbare batterijen

 Waarom werken enzymen meestal slechts op één substraat (of groep nauw verwante substraten)?
Waarom werken enzymen meestal slechts op één substraat (of groep nauw verwante substraten)?  Ben je veilig voor bliksem als het niet dondert?
Ben je veilig voor bliksem als het niet dondert?  Wat zou er gebeuren als een cel geen Golgi-lichamen had?
Wat zou er gebeuren als een cel geen Golgi-lichamen had?  Wat is farmaceutische wiskunde?
Wat is farmaceutische wiskunde?  Wat vormt de thermische energie van een object?
Wat vormt de thermische energie van een object?  Hoeveel kilometers zijn er in 5 nanometer?
Hoeveel kilometers zijn er in 5 nanometer?  Hoe een gebied in vierkante meters berekenen
Hoe een gebied in vierkante meters berekenen  Onderzoek naar menselijke factoren versnelt missieplanning
Onderzoek naar menselijke factoren versnelt missieplanning
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

