
Wetenschap
Chemisch evenwicht:reactant versus producthoeveelheden
Dit is waarom:
* Evenwicht is een dynamische toestand: Het is geen statische situatie waarin de reactie is gestopt. In plaats daarvan vinden de voorwaartse en achterwaartse reacties in hetzelfde tempo plaats . Dit betekent dat de snelheid waarmee producten worden gevormd gelijk is aan de snelheid waarmee reactanten worden gevormd.
* Relatieve bedragen: Hoewel de *snelheden* gelijk zijn, kunnen de *hoeveelheden* van reactanten en producten heel verschillend zijn. De relatieve hoeveelheden zijn afhankelijk van de evenwichtsconstante (K).
* K> 1: Is voorstander van producten. Bij evenwicht zullen er meer producten dan reactanten zijn.
* K <1: Geeft de voorkeur aan reactanten. Bij evenwicht zullen er meer reactanten zijn dan producten.
* K =1: Evenwicht wordt bereikt wanneer de hoeveelheden reactanten en producten gelijk zijn.
Voorbeeld: Denk aan een omkeerbare reactie waarbij A + B <-> C + D. Bij evenwicht is de reactie niet gestopt; het is alleen zo dat de vormingssnelheid van C en D gelijk is aan de vormingssnelheid van A en B. Er kunnen veel meer C en D aanwezig zijn, of veel meer A en B, afhankelijk van de waarde van K.
 Territoriaal beheer en bestuur van de Colombiaanse Amazone door inheemse volkeren
Territoriaal beheer en bestuur van de Colombiaanse Amazone door inheemse volkeren Geen El Niño? Geen probleem. Aarde sist tot bijna recordhitte
Geen El Niño? Geen probleem. Aarde sist tot bijna recordhitte Voorbeelden van secundaire verontreinigende stoffen
Voorbeelden van secundaire verontreinigende stoffen  Fotosynthese van planten bekijken... vanuit de ruimte
Fotosynthese van planten bekijken... vanuit de ruimte Materialisme en eenzaamheid:bestaat er werkelijk een vicieuze cirkel?
Materialisme en eenzaamheid:bestaat er werkelijk een vicieuze cirkel?
Hoofdlijnen
- Worden bloedcellen geproduceerd door mitose of meiose?
- Wat is de naam van de korte haarachtige structuur die op oppervlaktecellen wordt gevonden?
- Wat is het doel van een eukaryotische cel?
- Wat eet een marmot?
- De laboratoriumprocedure voor het kopiëren van geselecteerde segmenten van DNA is?
- Welk deel van de haarschacht wordt corticale cellen gemaakt?
- Uit welk deel van de hersenen komt cognitie?
- NOAA bevestigt vierde wereldwijde koraalverblekingsgebeurtenis
- Hoe boa's zichzelf behoeden voor verstikking bij het vernauwen en verteren van het avondeten
- Groen licht voor een nieuwe generatie dynamische materialen

- Kader om het pad van individuele koolstofatomen te volgen

- Nieuwe katalysator regelt activering van een koolstof-waterstofbinding
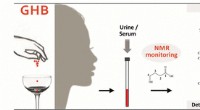
- De detectie van een date rape drug verbeteren
- Wetenschappers gebruiken coöperatieve actie van een ligand-tegenionsysteem voor duurzame etherproductie

 Wat is de golflengte van een rode ster?
Wat is de golflengte van een rode ster?  Palmbomen verspreiden zich naar het noorden. Hoe ver zullen ze gaan?
Palmbomen verspreiden zich naar het noorden. Hoe ver zullen ze gaan?  Wat wordt radium gebruikt voor vandaag?
Wat wordt radium gebruikt voor vandaag?  Wat betekent satellietbeeld?
Wat betekent satellietbeeld?  Hoe helpt groene vegetatie de hoeveelheid zuurstof in de atmosfeer te vergroten?
Hoe helpt groene vegetatie de hoeveelheid zuurstof in de atmosfeer te vergroten?  Welke term beschrijft alle veranderingen die plaatsvinden tijdens het leven van een organisme inclusief groei?
Welke term beschrijft alle veranderingen die plaatsvinden tijdens het leven van een organisme inclusief groei?  Wat is een biocrust?
Wat is een biocrust?  Waardoor zijn de continenten ontstaan? Nieuw bewijs wijst op gigantische asteroïden
Waardoor zijn de continenten ontstaan? Nieuw bewijs wijst op gigantische asteroïden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

