
Wetenschap
Atomaire lading begrijpen:winst en verlies van elektronen
* Elektronen verkrijgen: Wanneer een atoom een of meer elektronen krijgt, wordt het negatief geladen. Dit komt omdat elektronen een negatieve lading dragen. Een atoom dat een elektron krijgt, wordt een anion genoemd .
* Elektronen verliezen: Wanneer een atoom één of meer elektronen verliest, wordt het positief geladen. Dit komt omdat het atoom nu meer protonen (positief geladen deeltjes) heeft dan elektronen. Een atoom dat een elektron verliest, wordt een kation genoemd .
Belangrijkste punten om te onthouden:
* Het aantal protonen in een atoom bepaalt het atoomnummer en de elementidentiteit. Het blijft constant, zelfs wanneer een atoom elektronen wint of verliest.
* Elektronen bevinden zich in de buitenste schillen van een atoom en kunnen gemakkelijker worden gewonnen of verloren.
* Atomen hebben de neiging elektronen te winnen of te verliezen om een stabiele elektronenconfiguratie te bereiken, meestal door hun buitenste elektronenschil te vullen.
Voorbeeld:
* Een neutraal chlooratoom (Cl) heeft 17 protonen en 17 elektronen. Het kan één elektron winnen om een chloride-ion (Cl-) te worden, dat 17 protonen en 18 elektronen heeft, waardoor het een netto negatieve lading van -1 krijgt.
* Een neutraal natriumatoom (Na) heeft 11 protonen en 11 elektronen. Het kan één elektron verliezen om een natriumion (Na+) te worden, dat 11 protonen en 10 elektronen heeft, waardoor het een netto positieve lading van +1 krijgt.
Ionische bindingen begrijpen:
De neiging van atomen om elektronen te winnen of te verliezen om stabiliteit te bereiken, is de basis voor de vorming van ionische bindingen . Deze bindingen worden gevormd tussen tegengesteld geladen ionen (kationen en anionen) en zijn een belangrijke factor bij de vorming van veel verbindingen.
 Het verminderen van vervuiling door nutriënten helpt koraal bleken te weerstaan
Het verminderen van vervuiling door nutriënten helpt koraal bleken te weerstaan Avonturiers steken de Noordelijke IJszee over op ski's ondanks dunner wordend ijs
Avonturiers steken de Noordelijke IJszee over op ski's ondanks dunner wordend ijs Wat is de betekenis van leven en niet -dingen?
Wat is de betekenis van leven en niet -dingen?  G20 financiert fossiele brandstoffen $ 30 miljard per jaar onder de radar:analyse
G20 financiert fossiele brandstoffen $ 30 miljard per jaar onder de radar:analyse Regels om het brandstofverbruik van voertuigen te verhogen zullen meer goed dan kwaad doen, nieuwe studie toont
Regels om het brandstofverbruik van voertuigen te verhogen zullen meer goed dan kwaad doen, nieuwe studie toont
Hoofdlijnen
- Welke dieren hebben extern skelet?
- Wat doet genetisch materiaal in een cel?
- Een wiskundig principe legt uit hoe cellen zich met elkaar verbinden om weefsels en organen te vormen
- Genetisch gemodificeerd voedsel, wie moet het vertellen?
- De kwaliteit van bosbessen ontsluiten:de rol van cuticulaire was
- Onderzoek toont aan hoe cranberrysap bacteriën op moleculair niveau bestrijdt
- Hoe zou YPUB Definebiology DefineBiology DefinyBiology DefinyBiology definiëren?
- Een organisme kan niet overleven en zich reproduceren in zijn omgeving zonder?
- De rol van mutaties in evolutionaire processen
- Nieuwe zeolieten-zilverkatalysator verhoogt de oxidatie van formaldehyde bij lage temperaturen
- Een poreus porfyrine gebruiken om edele metalen terug te winnen uit elektronisch afval

- Anatomie van een acnebehandeling
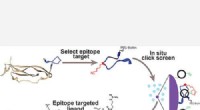
- Polymeren springen door hoepels op weg naar duurzame materialen

- Draagbare sensoren kunnen biotechnologie gebruiken om persoonlijke, milieugegevens
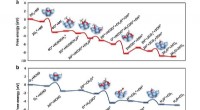
 Atoominterferometer chartert het traagheidsnavigatiepad van de marine om drift te verminderen
Atoominterferometer chartert het traagheidsnavigatiepad van de marine om drift te verminderen  Eerst een alg, dan een inktvis, enigmatisch fossiel is eigenlijk een vis
Eerst een alg, dan een inktvis, enigmatisch fossiel is eigenlijk een vis Welk effect hebben grote waterlichamen op het klimaat?
Welk effect hebben grote waterlichamen op het klimaat?  Chemische tracers ontwarren natuurlijk van methaanuitstoot in de landbouw
Chemische tracers ontwarren natuurlijk van methaanuitstoot in de landbouw De Europese Marslander:wat weten we?
De Europese Marslander:wat weten we?  Wat doet koper(II)sulfaat met de enzymactiviteit?
Wat doet koper(II)sulfaat met de enzymactiviteit?  Wat is de structuur die interne ondersteuning en bescherming biedt voor plantendierencellen?
Wat is de structuur die interne ondersteuning en bescherming biedt voor plantendierencellen?  Wat zijn enkele gevaren in het Carboon?
Wat zijn enkele gevaren in het Carboon?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

