
Wetenschap
Moleculaire verbindingen en elektrische geleidbaarheid:een uitgebreide uitleg
* Gebrek aan gratis laadproviders: Moleculaire verbindingen worden gevormd door het delen van elektronen tussen atomen om covalente bindingen te vormen. Deze elektronen worden stevig vastgehouden in het molecuul en kunnen niet vrij door het materiaal bewegen. Dit betekent dat er zeer weinig of geen gratis ladingsdragers zijn die elektrische stroom kunnen transporteren.
* Geen ionen: In tegenstelling tot ionische verbindingen, die geladen ionen hebben die vrij kunnen bewegen, hebben moleculaire verbindingen geen vrije ionen. Dit beperkt verder hun vermogen om elektriciteit te geleiden.
Uitzonderingen:
Hoewel de meeste moleculaire verbindingen slechte geleiders zijn, zijn er enkele uitzonderingen:
* Gesmolten of waterige oplossingen: Sommige moleculaire verbindingen, zoals water met opgeloste zuren of basen, kunnen elektriciteit geleiden als ze zich in vloeibare toestand bevinden. Dit komt omdat de opgeloste moleculen kunnen dissociëren in ionen, die vervolgens een stroom kunnen voeren.
* Grafiet: Grafiet is een vorm van koolstof met een unieke structuur die de beweging van elektronen binnen de lagen mogelijk maakt. Dit maakt grafiet een goede geleider van elektriciteit.
Samengevat:
Moleculaire verbindingen zijn over het algemeen slechte geleiders van elektriciteit omdat ze geen vrije ladingsdragers en ionen hebben. Er zijn echter enkele uitzonderingen, vooral in gevallen waarin de moleculen kunnen dissociëren in ionen of een unieke structuur hebben die elektronenbeweging mogelijk maakt.
 Vorm van vulkanische as beïnvloedt verontreiniging van waterbronnen in vulkanisch actieve gebieden
Vorm van vulkanische as beïnvloedt verontreiniging van waterbronnen in vulkanisch actieve gebieden Wat gebeurt er als de biodiversiteit is verloren?
Wat gebeurt er als de biodiversiteit is verloren?  Het verminderen van vervuiling door het wegvervoer kan planten helpen groeien
Het verminderen van vervuiling door het wegvervoer kan planten helpen groeien Wat zou een boom zeggen als het leven kreeg?
Wat zou een boom zeggen als het leven kreeg?  Roemeense bossen worden steeds meer bedreigd - samen met rangers
Roemeense bossen worden steeds meer bedreigd - samen met rangers
Hoofdlijnen
- Wat moet er gebeuren voor speciatie?
- De verschillende vormen van een eigenschap die Gene mogelijk heeft opgeroepen?
- Noem drie redenen waarom het zenuwstelsel een van de belangrijkste is in het lichaam?
- Waarom cellen meerdere tRNA-moleculen nodig hebben voor nauwkeurige eiwitsynthese
- Wat is genstroom?
- Wat is bacteriële suspensie?
- Wie heeft epigenetica ontdekt?
- Welk type moleculaire vergelijking zou helpen om te bepalen of schimmels nauwer gerelateerde planten of dieren zijn?
- Wat zijn de namen van twee typen waar weefsel gevonden in cnidarians?
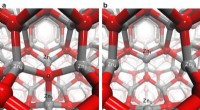
- Het is een valstrik - Onderzoekers identificeren het proces waardoor gaten vast komen te zitten in ZnO-nanodeeltjes
- Onderzoekers bepalen activeringsmechanisme van G-eiwit-gekoppelde receptoren

- Blauw versus rood lakmoespapier:hoe ze zuren en basen onthullen

- Hoe acrylplastic (PMMA) te vervaardigen:een gedetailleerde procesgids

- In de inkt:de wetenschap achter balpennen

 Dam in Libanon gepland bovenop breuklijn wekt angst op
Dam in Libanon gepland bovenop breuklijn wekt angst op Welke energietransformatie komt waarschijnlijk voor in een stoomijzer?
Welke energietransformatie komt waarschijnlijk voor in een stoomijzer?  Oxidatiegetallen voorspellen:een gids gebaseerd op periodieke trends
Oxidatiegetallen voorspellen:een gids gebaseerd op periodieke trends  Smalle plasmonische oppervlakteroosterresonanties geven de voorkeur aan een asymmetrische diëlektrische omgeving
Smalle plasmonische oppervlakteroosterresonanties geven de voorkeur aan een asymmetrische diëlektrische omgeving Hoe de natuurbescherming werkt
Hoe de natuurbescherming werkt  Chemicaliën die worden gebruikt in de chemie op de middelbare school
Chemicaliën die worden gebruikt in de chemie op de middelbare school Wat gebeurt er als je koperoxide laat reageren met en zuur?
Wat gebeurt er als je koperoxide laat reageren met en zuur?  Onderzoekers onderzoeken hulpbronnenschaarste en armoedevallen in de kust van Tanzania
Onderzoekers onderzoeken hulpbronnenschaarste en armoedevallen in de kust van Tanzania
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

