
Wetenschap
Protonen in zuur-base-reacties:een gedetailleerde uitleg
Zuren:
* Doneer protonen (H+): Zuren zijn stoffen die waterstofionen (H+), ook wel protonen genoemd, vrijgeven wanneer ze in water worden opgelost.
* Verhoog de H+-concentratie: De aanwezigheid van meer protonen in de oplossing maakt de oplossing zuurder.
Basis:
* Accepteer protonen (H+): Basen zijn stoffen die protonen (H+) accepteren wanneer ze in water worden opgelost.
* H+-concentratie verlagen: Basen verwijderen protonen uit de oplossing, waardoor de oplossing minder zuur (basisch) wordt.
Zuren en basen mengen:
* Neutralisatiereactie: Wanneer een zuur en een base reageren, ondergaan ze een neutralisatiereactie. Dit is een proces waarbij de protonen van het zuur (H+) reageren met de hydroxide-ionen van de base (OH-) om water (H2O) te vormen.
* Voorbeeld: HCl (zuur) + NaOH (base) -> NaCl (zout) + H2O (water)
* pH-verandering: De toevoeging van een zuur aan een base (of omgekeerd) resulteert in een verandering in de pH van de oplossing.
* Zuur + Base -> Neutralere pH :Als het zuur en de base in gelijke hoeveelheden aanwezig zijn, neutraliseren ze elkaar, wat resulteert in een neutrale oplossing met een pH dichtbij 7.
* Overtollig zuur -> Lagere pH: Als er een teveel aan zuur is, blijft de oplossing zuur bij een lagere pH.
* Overtollige base -> Hogere pH: Als er een overmaat aan base is, wordt de oplossing basisch bij een hogere pH.
Belangrijkste punten:
* Protonen zijn de belangrijkste spelers bij zuur-base-reacties.
* Zuren doneren protonen, basen accepteren ze.
* Neutralisatie is een proces waarbij protonen en hydroxide-ionen samenkomen om water te vormen.
*De pH van een oplossing weerspiegelt de concentratie van protonen.
Laat het me weten als je meer uitleg of voorbeelden van specifieke zuur-base-reacties wilt!
 Wat is abstract zelfstandig naamwoord van echt?
Wat is abstract zelfstandig naamwoord van echt?  Droogte treft vergrijzende boeren, slecht presterende boerderijen het moeilijkst
Droogte treft vergrijzende boeren, slecht presterende boerderijen het moeilijkst Gezonde bodem verhoogt het gewicht van de dieren
Gezonde bodem verhoogt het gewicht van de dieren Wetenschappers ontdekken een causaal verband tussen extreme hitte op afstand en de Canadese bosbranden in 2023
Wetenschappers ontdekken een causaal verband tussen extreme hitte op afstand en de Canadese bosbranden in 2023  Is het waar dat bomen regelmatig in grote aantallen uit een bos kunnen worden gevoed?
Is het waar dat bomen regelmatig in grote aantallen uit een bos kunnen worden gevoed?
Hoofdlijnen
- Uit de kleine teelballen van vliegen ontstaat nieuw inzicht in hoe genen ontstaan
- Eekhoorns en hamsters die in winterslaap zijn, zijn geëvolueerd om het minder koud te hebben
- Wat zijn de 2 soorten reproductieven?
- Een beter begrip van gewasopbrengsten onder klimaatverandering
- How Do Living Things Grow?
- Hoeveel water vormen de cellen van het organisme ongeveer?
- Hoe bidsprinkhaangarnalen vele vormen ontwikkelden met dezelfde krachtige stoot
- Wat zijn prokaryoten?
- Wat is een voorbeeld van wetenschap?
- Waterafstotend materiaal werpt af als een slang bij beschadiging

- Bioluminescente worm met ijzeren superkrachten

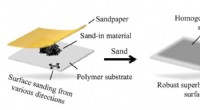
- Water kan dit geschuurde, gepoederde oppervlak niet raken
- Laser volgt therapieën, voedingsstoffen, gifstoffen

- Elektronische tong zorgt voor de snelle, goedkope detectie van vervalste honing

 Vergelijk en contrasteer. In welke opzichten lijken een substantieoplossing op elkaar en verschillen ze?
Vergelijk en contrasteer. In welke opzichten lijken een substantieoplossing op elkaar en verschillen ze?  Stoffige protoplanetaire schijven
Stoffige protoplanetaire schijven Hoe vertel je of een mineraal metaalachtig of niet-metaalachtig is?
Hoe vertel je of een mineraal metaalachtig of niet-metaalachtig is?  Bereken de gemiddelde afwijking
Bereken de gemiddelde afwijking  Creëer een realistisch Mars-model met eenvoudige papieren bordjes
Creëer een realistisch Mars-model met eenvoudige papieren bordjes  Menselijk benig labyrint gebruikt als indicator voor verspreiding vanuit Afrika
Menselijk benig labyrint gebruikt als indicator voor verspreiding vanuit Afrika Delen van het dier- en plantcellen hun betekenis?
Delen van het dier- en plantcellen hun betekenis?  Kunnen energiecentrales geen elektrische energie produceren of onwaar produceren?
Kunnen energiecentrales geen elektrische energie produceren of onwaar produceren?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

