
Wetenschap
Tin(IV)oxide (SnO₂):ionisch of covalent karakter?
* Verschil in elektronegativiteit: Tin (Sn) heeft een elektronegativiteit van 1,96, terwijl zuurstof (O) een elektronegativiteit heeft van 3,44. Het verschil is 1,48, wat significant genoeg is om op een ionbinding te wijzen.
* Metaal en niet-metaal: Tin is een metaal en zuurstof is een niet-metaal. Metalen hebben de neiging elektronen te verliezen, terwijl niet-metalen de neiging hebben elektronen te winnen, wat leidt tot de vorming van ionen en een ionische binding.
* Structuur: SnO₂ heeft een kristallijne structuur waarbij de tinionen (Sn⁴⁺) omgeven zijn door oxide-ionen (O²⁻). Deze opstelling is typerend voor ionische verbindingen.
Het is echter belangrijk op te merken:
* Hoewel SnO₂ voornamelijk ionisch is, is er een kleine mate van covalent karakter. Dit komt door het delen van de elektronendichtheid tussen de tin- en zuurstofatomen. Dit is gebruikelijk in veel verbindingen die als 'ionisch' worden beschouwd.
Dus hoewel SnO₂ als primair ionisch wordt beschouwd, is het niet geheel puur ionisch en heeft het een licht covalent karakter.
 Het oppompen van grondwater kan het arseengehalte in irrigatie- en drinkwater verhogen
Het oppompen van grondwater kan het arseengehalte in irrigatie- en drinkwater verhogen De geheime oorsprong van China's 40-jarenplan om een einde te maken aan de CO2-uitstoot
De geheime oorsprong van China's 40-jarenplan om een einde te maken aan de CO2-uitstoot Opinie:Trumps blijven klimaatontkenning en de branden van Californië
Opinie:Trumps blijven klimaatontkenning en de branden van Californië Plastic afval valt uiteen in nanodeeltjes, studie vondsten
Plastic afval valt uiteen in nanodeeltjes, studie vondsten Wat is een productiebos?
Wat is een productiebos?
Hoofdlijnen
- Kune Kune-biggen beschikken over sociale leervaardigheden en hebben een verbazingwekkend goed geheugen
- Talgachtige klieren behoren tot welke klasse?
- De concentratie van molecule X is groter in een cel dan buiten. Als de verwervingen uit zijn omgeving membraan moeten oversteken door middel van?
- Hoe verkrijgen verschillende organismen hun voedingsstoffen?
- Waarom zijn bacteriën en schimmels belangrijk voor het milieu?
- Welke cellulaire organel is vereist voor fotosynthese in eukaryotische cellen?
- Welke organel bereidt eiwitten in blaasjes om van het ene deel van een cel te transporteren?
- Ladderlopende sprinkhanen laten zien dat grote hersenen niet altijd de beste zijn
- Waarom was frenologie een rage in de Victoriaanse tijd?
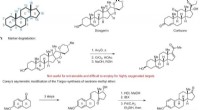
- Gestroomlijnd proces opent de ontwikkeling van geneesmiddelen voor een nieuwe klasse steroïden
- Nieuw op machine learning gebaseerd raamwerk kan leiden tot doorbraken in materiaalontwerp

- Levenscyclusanalyse lokaliseert duurzaamheidshotspots in biochemische productie

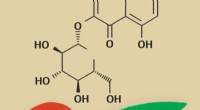
- Biochemici koppelen polyfenolen in perzikbladeren aan de antioxiderende werking van hun extract
- Crowdfunding van een consumeerbare bolvormige waterfles - de Ooho!

 Hoe ziet negatieve versnelling eruit in een grafiek van snelheid versus tijd?
Hoe ziet negatieve versnelling eruit in een grafiek van snelheid versus tijd?  Diverse levensonderhoud hielp veerkrachtige Levänluhta-mensen een klimaatramp te overleven
Diverse levensonderhoud hielp veerkrachtige Levänluhta-mensen een klimaatramp te overleven Nieuwe studie kraakt de code om de korrelgrootte te vergroten en de kalkvorming in rijst te verminderen
Nieuwe studie kraakt de code om de korrelgrootte te vergroten en de kalkvorming in rijst te verminderen Hoe energie te besparen in ons dagelijks leven
Hoe energie te besparen in ons dagelijks leven Is koolstof een vloeibare vaste stof of gas bij kamertemperatuur?
Is koolstof een vloeibare vaste stof of gas bij kamertemperatuur?  Survival of the least-fit:antiviraal middel richt zich selectief op de meest onaangename virussen
Survival of the least-fit:antiviraal middel richt zich selectief op de meest onaangename virussen Welk proces resulteert in bestuivers die specifiek zijn voor een bepaald type bloem?
Welk proces resulteert in bestuivers die specifiek zijn voor een bepaald type bloem?  Wanneer is Marble Arch gecreëerd?
Wanneer is Marble Arch gecreëerd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

