
Wetenschap
De pH van KH2PO4 begrijpen:een gedetailleerde uitleg
* KH2PO4 is een zout, geen sterk zuur of sterke base. Het wordt gevormd door de reactie van een zwak zuur (H3PO4, fosforzuur) en een sterke base (KOH, kaliumhydroxide).
* De pH van een zoutoplossing hangt af van de relatieve sterkte van het zuur en de base waaruit de oplossing is gevormd. In dit geval zal de oplossing van KH2PO4 enigszins zuur zijn, aangezien H3PO4 een zwak zuur is en KOH een sterke base.
* De pH is ook afhankelijk van de concentratie van de KH2PO4-oplossing.
Om de pH van een KH2PO4-oplossing te bepalen, hebt u het volgende nodig:
1. Ken de concentratie van de oplossing.
2. Gebruik de relevante evenwichtsconstanten: Je hebt de Ka-waarden voor de dissociatie van H3PO4 nodig om de waterstofionenconcentratie ([H+]) in de oplossing te berekenen.
Hier is een vereenvoudigde uitleg:
KH2PO4 in water zal gedeeltelijk dissociëren:
KH2PO4(aq) ⇌ K+(aq) + H2PO4-(aq)
Het H2PO4-ion kan zowel als zuur als als base werken, maar het is een zwakker zuur dan een base. Dit betekent dat de oplossing een iets hogere concentratie H+-ionen zal hebben dan OH-ionen, wat resulteert in een pH lager dan 7.
Om een nauwkeurige pH-waarde te krijgen, moet u een berekening uitvoeren met behulp van de juiste evenwichtsconstanten en de concentratie van de KH2PO4-oplossing.
 DNA-strengen gebruiken om nieuwe polymeermaterialen te ontwerpen
DNA-strengen gebruiken om nieuwe polymeermaterialen te ontwerpen Fotosynthese versus cellulaire ademhaling in elektronenstroom
Fotosynthese versus cellulaire ademhaling in elektronenstroom Wat is de bron van koolstof voor ademhaling?
Wat is de bron van koolstof voor ademhaling?  Antwoord op bacteriële antibioticaresistentie kan worden gevonden in planten
Antwoord op bacteriële antibioticaresistentie kan worden gevonden in planten Loodchloridesynthese:de reactie met natrium en nitraat begrijpen
Loodchloridesynthese:de reactie met natrium en nitraat begrijpen
 Zijn bugs mensen lastig of andersom? Onderzoek brengt enkele verrassingen aan het licht
Zijn bugs mensen lastig of andersom? Onderzoek brengt enkele verrassingen aan het licht  Welk bioom heeft het grootste aantal planten- en diersoorten in een bepaald gebied?
Welk bioom heeft het grootste aantal planten- en diersoorten in een bepaald gebied?  Waar zijn alle zwaluwen gebleven?
Waar zijn alle zwaluwen gebleven?  NASA ziet tyfoon Maria aan land komen in China
NASA ziet tyfoon Maria aan land komen in China Stikstof, fosfor uit meststoffen en uitwerpselen van huisdieren die stedelijk water vervuilen
Stikstof, fosfor uit meststoffen en uitwerpselen van huisdieren die stedelijk water vervuilen
Hoofdlijnen
- Het enzym dat een kanaal vormt in het binnenmembraan van mitochondria en fosforyleert ADP is?
- Wat zijn de waarneembare eigenschappen van een organisme?
- Veel microscopische organismen die moeilijk te classificeren waren geplaatst in het koninkrijk?
- Wat is de functie van een ui -celkern?
- Onderzoekers tonen aan dat de lengte van telomeren de levensverwachting in het wild voorspellen
- Parasitaire mieren veranderen de manier waarop gevangenen nestgenoten herkennen
- Alaska:de ultieme bestemming voor het spotten van Amerikaanse zeearenden – waar te gaan en hoe je ze kunt spotten
- Hoe het blokkeren van celwandvorming de bacteriële deling stopt
- Waarom lijken organismen op elkaar?
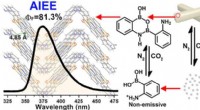
- Nieuw door aggregatie geïnduceerd aromatisch molecuul met verbeterde emissie ontdekt
- Wetenschappers gebruiken neutronen om te proberen zich beter te ontwikkelen, goedkopere tandheelkundige restauraties
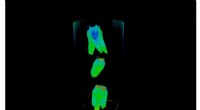
- De kracht van elektriciteitproducerende bacteriën benutten voor programmeerbare biohybriden

- Chemici maken harde kunststoffen recyclebaar

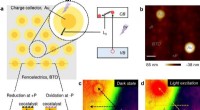
- Wetenschappers stellen nieuwe ladingsscheidingsstrategie voor in ferro-elektrische fotokatalysatoren
 Wat zijn de twee belangrijkste soorten energiegolven?
Wat zijn de twee belangrijkste soorten energiegolven?  Wat was de langste tijd doorgebracht aan de maan?
Wat was de langste tijd doorgebracht aan de maan?  Heeft een infrarood min of meer energie dan ultraviolette golf?
Heeft een infrarood min of meer energie dan ultraviolette golf?  Objecten die vallen, hebben een constante versnelling op de naam WAT?
Objecten die vallen, hebben een constante versnelling op de naam WAT?  Barium Nitrate & Sodium Sulphate
Barium Nitrate & Sodium Sulphate Wat is de naam van Compound NA4SI?
Wat is de naam van Compound NA4SI?  Welke kracht werkt op een space shuttle als deze versnelt?
Welke kracht werkt op een space shuttle als deze versnelt?  Waterstofatomen in ammoniumcarbonaat:een stapsgewijze berekening
Waterstofatomen in ammoniumcarbonaat:een stapsgewijze berekening
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

