
Wetenschap
Berekening van de pH van NaOH-oplossingen:0,1M en 0,05M
De concepten begrijpen
* NaOH (natriumhydroxide): Een sterke base die volledig dissocieert in water en hydroxide-ionen (OH-) en natriumionen (Na+) produceert.
* pH: Een maatstaf voor de zuurgraad of basiciteit van een oplossing. Het wordt berekend met behulp van de formule:
pH =-log[H+]
waarbij [H+] de concentratie waterstofionen is.
* pOH: Een maat voor de concentratie hydroxide-ionen. Het wordt berekend met behulp van de formule:
pOH =-log[OH-]
* Verband tussen pH en pOH:
pH + pOH =14
Berekeningen
1. 0,1 M NaOH
* Zoek [OH-] :Omdat NaOH volledig dissocieert, is de concentratie van OH-ionen gelijk aan de concentratie van NaOH, die 0,1 M is.
* Bereken pOH:
pOH =-log(0,1) =1
* Bereken de pH:
pH =14 - pOH =14 - 1 =13
Daarom is de pH van 0,1 M NaOH 13.
2. 0,05 M NaOH
* Zoek [OH-] :De concentratie OH-ionen is gelijk aan de concentratie NaOH, namelijk 0,05 M.
* Bereken pOH:
pOH =-log(0,05) =1,3
* Bereken de pH:
pH =14 - pOH =14 - 1,3 =12,7
Daarom is de pH van 0,05 M NaOH 12,7.
Belangrijkste punten
*NaOH-oplossingen hebben een hoge pH vanwege de aanwezigheid van een hoge concentratie hydroxide-ionen (OH-).
* Hoe hoger de concentratie NaOH, hoe hoger de pH.
* Sterke basen zoals NaOH dissociëren volledig in water, waardoor de berekeningen eenvoudig zijn.
 Soorten eetbare paddestoelen in Texas
Soorten eetbare paddestoelen in Texas Nieuwe satelliettechnologie biedt een meer gedetailleerde kaart van bewegende Antarctische gletsjers
Nieuwe satelliettechnologie biedt een meer gedetailleerde kaart van bewegende Antarctische gletsjers NASA ziet Atlantische subtropische storm Melissa vormen voor de kust van New England
NASA ziet Atlantische subtropische storm Melissa vormen voor de kust van New England Los Angeles:Hollywood, palmbomen en stedelijke olievelden
Los Angeles:Hollywood, palmbomen en stedelijke olievelden Carbon Cycling in Aquatic Ecosystems
Carbon Cycling in Aquatic Ecosystems
Hoofdlijnen
- Hoe verschilt de biologische evolutie van chemische evolutie?
- Welk micro -organisme wordt beschreven in de volgende passage zijn ze kleine cellen. Hun cellen bevatten geen kern maar hebben celwand.
- Critici van positieve actie schilderen Aziatische Amerikanen af als de 'modelminderheid'. Waarom dat niet waar is
- Deze regio in een kern is waar rRNA produceert?
- Geschiedenis van de aarde: tijdlijn, proces en feiten
- Hoe ingewikkelde patronen ontstaan in zich ontwikkelende weefsels
- Vrijwilligers bevrijden een Australische rivier van het ligusterprobleem en versterken onderweg de gemeenschap
- Eukaryotische cellen verschillen van prokaryotische cellen?
- Wat zijn twee belangrijke componenten van het cytoskelet?
- Wetenschappers ID-enzym voor het maken van belangrijke industriële chemicaliën in planten
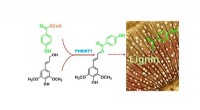
- Nieuwe topologische materialen kunnen meerdere elektrische eigenschappen hebben

- Onderzoekers observeren het schakelen van Ras-eiwit in detail

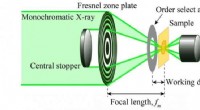
- Een scanning transmissie-röntgenmicroscoop voor analyse van chemische toestanden van lithium
- Studie update etnobotanie, fytochemie en farmacologie van het geslacht Didymocarpus Wall.

 Onderzoeksteam ontwikkelt nieuwe klasse zachte materialen
Onderzoeksteam ontwikkelt nieuwe klasse zachte materialen Wat was de naam van het eerste ruimtevaartuig om op de maan te landen?
Wat was de naam van het eerste ruimtevaartuig om op de maan te landen?  Wat zit er in de lucht? Er komt meer bij kijken dan we dachten
Wat zit er in de lucht? Er komt meer bij kijken dan we dachten  Inzicht in de relatie tussen elektronegativiteit en ionisatie-energie
Inzicht in de relatie tussen elektronegativiteit en ionisatie-energie  Hoe aardbevingsbestendige gebouwen werken
Hoe aardbevingsbestendige gebouwen werken  Wat voor soort helling heeft versnelling?
Wat voor soort helling heeft versnelling?  Onderzoekers gebruiken AI om de beeldkwaliteit van metalen camera's te verbeteren
Onderzoekers gebruiken AI om de beeldkwaliteit van metalen camera's te verbeteren  Stort fotosynthese energie op in de aarde die rekening wordt gehouden voor levende organismen?
Stort fotosynthese energie op in de aarde die rekening wordt gehouden voor levende organismen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

