
Wetenschap
Plutoniumverbindingen:eigenschappen, gebruik en stabiliteit
Plutonium kan echter verschillende verbindingen vormen, waarvan sommige:
Oxiden:
* Plutoniumdioxide (PuO₂): Het meest voorkomende en stabiele oxide van plutonium. Het is een zwarte, keramiekachtige vaste stof die wordt gebruikt als brandstof in kernreactoren.
* Plutoniumtrioxide (PuO₃): Minder stabiel dan plutoniumdioxide.
Halogeniden:
* Plutoniumfluoride (PuF₃, PuF₄, PuF₆): Fluoriden zijn vooral belangrijk voor nucleaire toepassingen.
* Plutoniumchloride (PuCl₃):
* Plutoniumbromide (PuBr₃):
Andere verbindingen:
* Plutoniumnitride (PuN): Gebruikt als brandstof in kernreactoren.
* Plutoniumcarbide (PuC): Wordt ook gebruikt als brandstof in kernreactoren.
* Plutoniumhydride (PuH₃):
* Plutoniumlegeringen: Legeringen met andere metalen, zoals uranium, worden gebruikt in kernwapens en reactoren.
Het is belangrijk op te merken dat het werken met plutoniumverbindingen gespecialiseerde faciliteiten en apparatuur vereist vanwege de hoge radioactiviteit en toxiciteit van het element.
 Uit onderzoek blijkt dat klimaatverandering 10% heeft toegevoegd aan Ians regenval
Uit onderzoek blijkt dat klimaatverandering 10% heeft toegevoegd aan Ians regenval GPM vindt zware regen in een band die zich in de tropische storm Miriam wikkelt
GPM vindt zware regen in een band die zich in de tropische storm Miriam wikkelt Nieuw-Zeelands White Island zal waarschijnlijk opnieuw uitbarsten, maar een nieuw waarschuwingssysteem kan urenlang waarschuwen en levens redden
Nieuw-Zeelands White Island zal waarschijnlijk opnieuw uitbarsten, maar een nieuw waarschuwingssysteem kan urenlang waarschuwen en levens redden Onderzoek van internationale archeologen onthult diepere en meer wijdverbreide wortels van het Antropoceen
Onderzoek van internationale archeologen onthult diepere en meer wijdverbreide wortels van het Antropoceen Wat wordt bedoeld met lagere soortendiversiteit?
Wat wordt bedoeld met lagere soortendiversiteit?
Hoofdlijnen
- Hoe ondergaat een dierencel cytokinese?
- Is een uiencel van autotrofe of heterotrofe organisme?
- Wat is de definitie van pyrogenen?
- Welke 2 stoffen bestaan chromosomen?
- Enzymen kunnen de sleutel zijn om te begrijpen hoe DNA muteert, vinden kwantumbiologen
- Hoe kan één celkloon worden verkregen uit een cultuur?
- In welke levensfase komt mitose sneller voor?
- Hoe kopiëren cellen zichzelf?
- Onderzoek ontrafelt het mysterie van hoe vroege dieren de ijstijd overleefden
- Snelle screening op potentiële nieuwe katalysatoren

- Ecologische energie-accu gemaakt van vanilline

- Een nieuwe manier om MXene-films te maken die elektromagnetische interferentie blokkeren

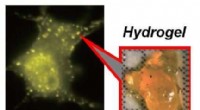
- Onderzoekers rapporteren allereerste eiwithydrogels gemaakt in levende cellen
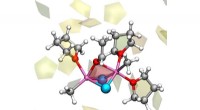
- De 120 jaar oude cold case voor de Grignard-reactie is eindelijk opgelost
 Hoe Tangential Force te berekenen
Hoe Tangential Force te berekenen  Op welke temperatuur bevriest het ongelode gas?
Op welke temperatuur bevriest het ongelode gas?  Als de tijd stopt met de snelheid van het licht, hoe bewegen fotonen?
Als de tijd stopt met de snelheid van het licht, hoe bewegen fotonen?  Microben die onafhankelijk leven maar samenwerken en voedingsstoffen delen hoe het wordt genoemd?
Microben die onafhankelijk leven maar samenwerken en voedingsstoffen delen hoe het wordt genoemd?  Welke metabole route heeft de meeste ATP?
Welke metabole route heeft de meeste ATP?  Welke geometrische vorm is C2H4?
Welke geometrische vorm is C2H4?  Noordelijkste koraalrif ter wereld in Japan verbleekt
Noordelijkste koraalrif ter wereld in Japan verbleekt De verkleuring en het verval van oppervlakte rotsmateriaal is een gevolg van?
De verkleuring en het verval van oppervlakte rotsmateriaal is een gevolg van?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

