
Wetenschap
Geleidbaarheid van kaliumchloride:vaste versus gesmolten toestand uitgelegd
Solid State:
* Ionische binding: Kaliumchloride is een ionische verbinding. Dit betekent dat het bij elkaar wordt gehouden door sterke elektrostatische aantrekkingen tussen positief geladen kaliumionen (K+) en negatief geladen chloride-ionen (Cl-).
* Vaste ionen: In de vaste toestand zijn deze ionen gerangschikt in een stijve, kristallijne roosterstructuur. Ze zijn stevig gebonden aan hun posities en kunnen zich niet vrij bewegen.
* Geen gratis kostenaanbieders: Omdat de ionen op hun plaats zitten, zijn er geen vrije ladingen beschikbaar om elektrische stroom te geleiden. Zelfs als je een elektrisch veld aanbrengt, kunnen de ionen niet bewegen en zo een ladingsstroom creëren.
Gesmolten toestand (vloeistof):
* Gebroken rooster: Wanneer kaliumchloride smelt, verzwakken de sterke ionische bindingen en wordt het kristalrooster afgebroken.
* Mobiele ionen: De ionen kunnen nu willekeurig door de vloeistof bewegen. Deze beweging is essentieel voor de elektrische geleiding.
* Geleidbaarheid: Wanneer een elektrisch veld wordt aangelegd op het gesmolten KCl, migreren de vrije kalium- en chloride-ionen naar de tegengesteld geladen elektroden. Deze beweging van geladen deeltjes vormt een elektrische stroom.
Samengevat:
* Vaste KCl: Vaste ionen, geen vrije ladingsdragers, geen geleidbaarheid.
* Gesmolten KCl: Vrije ionen, mobiele ladingsdragers, goede geleiding.
Hoofdlijnen
- Waarom verlaten zoveel vrouwen de biologie?
- Wat speelt een rol bij jouw lichaamstype?
- Wat is biotictechnologie?
- Hoe zoutwaterconsumptie tot uitdroging leidt:het osmose-effect
- Wat is de rol die van vitaal belang is van schimmels zoals Rhizopus in de natuur?
- Noem twee planten die groeien uit sporen en geen zaden?
- Waarom trilt de motor?
- Hoe definieer je haat?
- Differentiëren de termen homozygoot en heterozygoot?
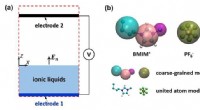
- Onderzoek verbetert theorieën over ionenverdamping en prestaties van elektrospraytoepassingen
- Wetenschappers werken aan biologisch afbreekbaar plastic van zonlicht

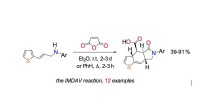
- Chemici suggereren een nieuwe manier om steroïde-analogen te synthetiseren
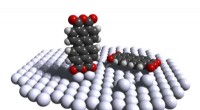
- Lastige prestatie met opstaand molecuul
- Hoe u een hoogwaardige elektrolytoplossing voor batterijen kunt bereiden

 Speelt druk een rol bij de vorming van metamorfe rotsen?
Speelt druk een rol bij de vorming van metamorfe rotsen?  Wat doet desinfectiemiddel als chemische stof?
Wat doet desinfectiemiddel als chemische stof?  Een nieuwe telescoop vergroot het zicht van de Big Bear Solar Observatory op de zon
Een nieuwe telescoop vergroot het zicht van de Big Bear Solar Observatory op de zon Goedkope techniek voor het etsen van nanogaten in silicium zou de basis kunnen vormen voor nieuwe filtratie- en nanofotonische apparaten
Goedkope techniek voor het etsen van nanogaten in silicium zou de basis kunnen vormen voor nieuwe filtratie- en nanofotonische apparaten DNA in dunne draadachtige vorm wordt aangeroepen?
DNA in dunne draadachtige vorm wordt aangeroepen?  Eerste veldmetingen lachgasisotopen
Eerste veldmetingen lachgasisotopen Antarctisch Schiereiland warmt op door hitte in Tasmanzee
Antarctisch Schiereiland warmt op door hitte in Tasmanzee JAXA gebruikt waterflestechnologie voor monsterretourmissies vanuit het ISS
JAXA gebruikt waterflestechnologie voor monsterretourmissies vanuit het ISS
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


