
Wetenschap
Calciumcarbonaat en zoutzuurreactie:vergelijking en uitleg
CaCO3 (s) + 2HCl (aq) → CaCl2 (aq) + H2 O (l) + CO2 (g)
Dit is wat de vergelijking vertegenwoordigt:
* CaCO3 (s) - Vast calciumcarbonaat (krijt)
* 2HCl (water) - Waterig zoutzuur
* CaCl2 (aq) - Waterig calciumchloride
* H2 O (l) - Vloeibaar water
* CO2 (g) - Gasvormig kooldioxide
Uitleg:
De reactie tussen krijt en zoutzuur is een klassieke zuur-base-reactie. Het zoutzuur (HCl) werkt als een zuur en doneert een proton (H+) aan het calciumcarbonaat (CaCO3 ). Dit resulteert in de vorming van calciumchloride (CaCl2 ), water (H2 O), en kooldioxide (CO2 ).
Opmerkingen:
Wanneer krijt reageert met zoutzuur, zie je het volgende:
* Bruisend: Door het vrijkomen van koolstofdioxidegas gaat de oplossing bruisen.
* Oplossen: Het krijt zal oplossen als het reageert met het zuur.
* Warmte: De reactie is exotherm, wat betekent dat er warmte vrijkomt.
Belangrijke opmerkingen:
* Deze reactie is een neutralisatiereactie, wat betekent dat een zuur en een base reageren om zout en water te vormen.
*De reactie is een goed voorbeeld van een chemische reactie waarbij een gas ontstaat.
* De reactie wordt vaak gebruikt in scheikundige experimenten om de principes van zuur-base-reacties aan te tonen.
 Welk element wordt gebruikt in munten en structurele materialen?
Welk element wordt gebruikt in munten en structurele materialen?  Levensduur van betonconstructies verlengd door een koolstoftextiel
Levensduur van betonconstructies verlengd door een koolstoftextiel Welke elementen heeft het samengestelde ijzeroxide?
Welke elementen heeft het samengestelde ijzeroxide?  Zuurstofatomen in het zuurstofgas geproduceerd door fotosynthese komt uit wat?
Zuurstofatomen in het zuurstofgas geproduceerd door fotosynthese komt uit wat?  Welke vaste stof vormt een uitzondering op de regel dat vaste stoffen een hogere dichtheid hebben dan vloeistoffen?
Welke vaste stof vormt een uitzondering op de regel dat vaste stoffen een hogere dichtheid hebben dan vloeistoffen?
 Wat is de relatie tussen ecologisch en opvolgingsevenwicht in een ecosysteem?
Wat is de relatie tussen ecologisch en opvolgingsevenwicht in een ecosysteem?  Kunnen we dinosaurussen doen herrijzen uit fossiele embryo's?
Kunnen we dinosaurussen doen herrijzen uit fossiele embryo's?  Hoe klimaatverandering nieuwe epidemieën aan het licht zou kunnen brengen
Hoe klimaatverandering nieuwe epidemieën aan het licht zou kunnen brengen  Om verbonden te zijn met de natuur, kinderen hebben buiten eenzame activiteiten nodig
Om verbonden te zijn met de natuur, kinderen hebben buiten eenzame activiteiten nodig Indische Oceaan veroorzaakt droogte en hittegolven in Zuid-Amerika
Indische Oceaan veroorzaakt droogte en hittegolven in Zuid-Amerika
Hoofdlijnen
- Brandstof voor de toekomst:wetenschappers promoten nieuwe methode voor de productie van algenwaterstof
- Glucose en zuurstof zijn de producten van wat?
- Waar bevindt het celmembraan zich in een cel?
- 'Welke dag is het ook alweer?' De psychologie van dinsdag
- Nieuw voorspellingsmodel voor kantelpunten biedt inzicht in afnemende bijenvolken
- Is het Elkhorn Coral een Carnovore Omnivore of Herbivore?
- Welke cytoskeletale eiwitten zijn belangrijke bestanddelen van de contractiele structuren die splitsing vormen die betrokken zijn bij cytokinese van diercellen?
- Bacterieel controlemechanisme voor aanpassing aan veranderende omstandigheden
- Heeft een bladcel chloroplast?
- Onderzoekers realiseren 4D-geprint materiaal

- Een chemische aanwijzing voor hoe het leven op aarde begon

- Hoe het percentage ionisatie van zwakke zuren en basen te berekenen

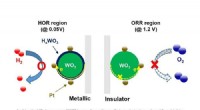
- Wetenschappers lossen een duurzaamheidsprobleem op in brandstofcellen voor waterstofauto's
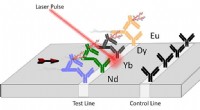
- Nieuwe technologie voor detectie van pathogenen aangedreven door lasers
 Spelen planten en dieren een rol in de watercycli van de watercool?
Spelen planten en dieren een rol in de watercycli van de watercool?  Meisjes zien wetenschap minder snel als een levensvatbare carrière wanneer ze les krijgen naast wetenschappelijk zelfverzekerde klasgenoten
Meisjes zien wetenschap minder snel als een levensvatbare carrière wanneer ze les krijgen naast wetenschappelijk zelfverzekerde klasgenoten Welk percentage van de naties energie wordt verstrekt door thermisch?
Welk percentage van de naties energie wordt verstrekt door thermisch?  Ingenieurs begrijpen nu hoe complexe koolstofnanostructuren ontstaan
Ingenieurs begrijpen nu hoe complexe koolstofnanostructuren ontstaan  Waarom moeten levende wezens mitose moeten plaatsvinden?
Waarom moeten levende wezens mitose moeten plaatsvinden?  De massa van moleculen meten op nanoschaal
De massa van moleculen meten op nanoschaal Nano-emulsievaccins zijn steeds veelbelovender
Nano-emulsievaccins zijn steeds veelbelovender  Wordt het weer slechter in 2018? Wat de experts zeggen
Wordt het weer slechter in 2018? Wat de experts zeggen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

