
Wetenschap
Li+ Ion-elektronenconfiguratie:kern- en valentie-elektronen uitgelegd
Lithiumatoom (Li)
* Atoomnummer: 3 (wat betekent dat het 3 protonen en 3 elektronen heeft)
* Elektronenconfiguratie: 1s² 2s¹
* Kernelektronen: 2 (de elektronen in de 1s-orbitaal)
* Valentie-elektronen: 1 (het elektron in de 2s-orbitaal)
Lithiumion (Li+)
* Formatie: Lithium verliest zijn ene valentie-elektron om een stabiele, edelgasconfiguratie zoals helium (1s²) te bereiken.
* Elektronenconfiguratie: 1s²
* Kernelektronen: 2 (de elektronen in de 1s-orbitaal)
* Valentie-elektronen: 0 (het heeft zijn enige valentie-elektron verloren)
Belangrijkste punten
* Kernelektronen zijn de elektronen in de binnenste schillen van een atoom. Ze zijn over het algemeen niet betrokken bij chemische binding.
* Valentie-elektronen zijn de elektronen in de buitenste schil van een atoom. Ze zijn betrokken bij chemische bindingen en bepalen de reactiviteit van een element.
* Wanneer lithium zijn valentie-elektron verliest, wordt het een positief geladen ion (Li+) met een volledige buitenschil, waardoor het stabieler wordt.
 Een lage prijs, hoogrenderende katalysator die koolstofdioxide omzet in andere chemicaliën
Een lage prijs, hoogrenderende katalysator die koolstofdioxide omzet in andere chemicaliën Welke warmte -energie overgedragen door een stof door direct moleculair contact?
Welke warmte -energie overgedragen door een stof door direct moleculair contact?  Netto ionische vergelijking voor ijzernitraat en ammoniak?
Netto ionische vergelijking voor ijzernitraat en ammoniak?  Een stap dichter bij de realiteit
Een stap dichter bij de realiteit Welke van de volgende verwijdert koolstof uit de atmosfeer?
Welke van de volgende verwijdert koolstof uit de atmosfeer?
 Klimaatverandering en de ineenstorting van Angkor Wat
Klimaatverandering en de ineenstorting van Angkor Wat Wanneer is context van belang bij productbeoordelingen?
Wanneer is context van belang bij productbeoordelingen?  Satellieten, supercomputers, en machine learning bieden realtime gegevens over het gewastype
Satellieten, supercomputers, en machine learning bieden realtime gegevens over het gewastype Blootstelling aan luchtvervuiling bij vrouwen in Mozambique sterk geïntensiveerd door gebruik van petroleumlampen
Blootstelling aan luchtvervuiling bij vrouwen in Mozambique sterk geïntensiveerd door gebruik van petroleumlampen Wat betekent het woord grond in de wetenschap?
Wat betekent het woord grond in de wetenschap?
Hoofdlijnen
- Behandeling van antibioticaresistente infecties met peptiden geïnspireerd op menselijk speeksel
- De COVID-19-pandemie veranderde onze patronen en gedragingen, wat op zijn beurt gevolgen had voor de natuur
- Wat gebeurt er als twee of meer organismen naast elkaar bestaan in dezelfde niche?
- Identificatie van een nieuwe familie van op licht reagerende eiwitten
- Hoe gendergelijkheid te behouden via de geslachtschromosomen
- Noem de modus van voeding in ronde worm en Plasmodium?
- Waarom wordt het proces dat plaatsvindt in een mitochondrion die vaak wordt beschreven als tegengesteld aan Taht -chloroplast?
- Het Snap Bean-paneel onthult de variabiliteit in fenotypes van blad- en peulkleuren
- Zijn embryonale stamcellen en kunstmatige gelijkwaardig?
- Iridium-gekatalyseerde Z-retentieve asymmetrische allylische substitutiereacties
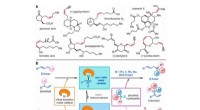
- Guardians of the Ring - Onderzoekers onthullen de structuur van eiwitten die betrokken zijn bij ontstekingsziekten
- 2D-kristallen die voldoen aan 3D-curven veroorzaken spanning voor technische kwantumapparaten

- Alternatieven vinden voor diamanten om te boren
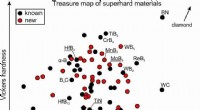
- Defecten in nanoporeuze materialen temmen om ze nuttig te gebruiken
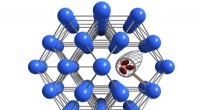
 Ontdekking van supergeleiding van bismut bij extreem lage temperatuur brengt theorie in gevaar
Ontdekking van supergeleiding van bismut bij extreem lage temperatuur brengt theorie in gevaar Bestuderen van argongas gevangen in een tweedimensionale reeks kleine kooien
Bestuderen van argongas gevangen in een tweedimensionale reeks kleine kooien Welke meet de snelheid van welke energie wordt overgedragen?
Welke meet de snelheid van welke energie wordt overgedragen?  Wat is de vorm van formatie SO2?
Wat is de vorm van formatie SO2?  Is een volle maan hetzelfde als 1 veertien dagen?
Is een volle maan hetzelfde als 1 veertien dagen?  Hoe bananen kunnen worden gebruikt om de plasticafvalcrisis te bestrijden
Hoe bananen kunnen worden gebruikt om de plasticafvalcrisis te bestrijden  Waarom planeten een afgeplatte bolvorm aannemen
Waarom planeten een afgeplatte bolvorm aannemen  Wat is de relatie tussen snelheidsnelheid en versnelling?
Wat is de relatie tussen snelheidsnelheid en versnelling?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

