
Wetenschap
Zuurstof vereist voor de verbranding van benzeen:een stapsgewijze berekening
1. Evenwichtige chemische vergelijking:
Bij de verbranding van benzeen (C₆H₆) ontstaat kooldioxide (CO₂) en water (H₂O):
2 C₆H₆ + 15 O₂ → 12 CO₂ + 6 H₂O
2. Bereken het aantal mol benzeen:
* Molaire massa van benzeen (C₆H₆) =78,11 g/mol
* Mol benzeen =(39 g) / (78,11 g/mol) =0,5 mol
3. Bepaal het benodigde aantal mol zuurstof:
* Uit de uitgebalanceerde vergelijking blijkt dat voor 2 mol benzeen 15 mol zuurstof nodig is.
* Mol benodigde zuurstof =(0,5 mol benzeen) * (15 mol O₂ / 2 mol benzeen) =3,75 mol O₂
4. Converteer mol zuurstof naar liters bij STP:
* Bij standaardtemperatuur en -druk (STP) neemt 1 mol van elk ideaal gas 22,4 liter in beslag.
* Liter zuurstof =(3,75 mol O₂) * (22,4 L/mol) =84 liter
Voor de verbranding van 39 gram vloeibare benzeen bij STP is dus ongeveer 84 liter zuurstof nodig.
 Edelstenen gevonden in Wisconsin
Edelstenen gevonden in Wisconsin  Wat is het zelfstandig naamwoord voor warmte?
Wat is het zelfstandig naamwoord voor warmte?  Volgens theorie van natuurlijke selectie zijn individuen die overleven degenen die het beste zijn aangepast voor hun omgeving waarover overleving is afhankelijk?
Volgens theorie van natuurlijke selectie zijn individuen die overleven degenen die het beste zijn aangepast voor hun omgeving waarover overleving is afhankelijk?  Experiment met waterdeling suggereert dat mensen hun eigen overleving op de eerste plaats zetten
Experiment met waterdeling suggereert dat mensen hun eigen overleving op de eerste plaats zetten Het niet-bevroren watergehalte beïnvloedt de thermische-hydromechanische eigenschappen van bevroren grond
Het niet-bevroren watergehalte beïnvloedt de thermische-hydromechanische eigenschappen van bevroren grond
Hoofdlijnen
- Wat zijn de 2 soorten cellen?
- VS voorstel zou het doden van adelaars toestaan naarmate hernieuwbare energiebronnen toenemen
- Wat is de eenvoudigste cel?
- De mutaties die fokkers in organismen induceren, worden doorgegeven aan de organismen?
- Wat is een analogie van de celstad voor ribosomen?
- Hoe beschrijf je de vorm van structuur -DNA?
- Wat doet de kern in het lichaam?
- Het ontrafelen van de redenen waarom massale uitstervingen plaatsvinden
- Wat voor soort organismen bezitten eukaryotische cellen?
- Verbeterde katalysator kan zich vertalen in winst in de petrochemische productie

- Biosensoren verlichten cellulaire signaalprocessen

- Hiërarchisch poreuze koolstofnetwerken ingebed met enkele ijzerplaatsen voor efficiënte zuurstofreductie
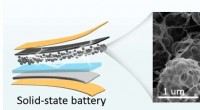
- Van broeikasgassen tot plastic:nieuwe katalysator voor recycling koolstofdioxide ontdekt

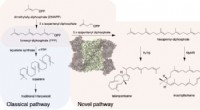
- Nieuw type triterpenen ontdekt
 Problemen bij de introductie van een nieuwe soort in een ecosysteem?
Problemen bij de introductie van een nieuwe soort in een ecosysteem?  Lysosomen:de recyclingcentra van de cel - hoe ze werken
Lysosomen:de recyclingcentra van de cel - hoe ze werken  Hoe berekent u hoeveel gram water wordt geproduceerd uit 22,1 zuurstof?
Hoe berekent u hoeveel gram water wordt geproduceerd uit 22,1 zuurstof?  Hoeveel verbindingen onderscheiden zich van elementen en mengsels?
Hoeveel verbindingen onderscheiden zich van elementen en mengsels?  Waarom stenen zich tot bodem vormen?
Waarom stenen zich tot bodem vormen?  Is de rol van centrosomen nodig voor mitose?
Is de rol van centrosomen nodig voor mitose?  Hoeveel vierkante decimeters maakt 1 meter?
Hoeveel vierkante decimeters maakt 1 meter?  Transplantatiebeschadigend virus komt in beeld
Transplantatiebeschadigend virus komt in beeld
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

