
Wetenschap
Anionvorming begrijpen:waarom niet-metalen elektronen verkrijgen
* Elektronegativiteit: Dit is een maatstaf voor het vermogen van een atoom om elektronen naar zich toe te trekken in een chemische binding. Niet-metalen hebben over het algemeen een hogere elektronegativiteit dan metalen.
* Bondvorming: Wanneer een niet-metaalatoom interageert met een metaalatoom, trekt de sterkere aantrekkingskracht van het niet-metaal op elektronen de gedeelde elektronen dichter naar zichzelf toe.
* Elektronenoverdracht: Deze onbalans in het delen van elektronen brengt effectief een elektron over van het metaalatoom naar het niet-metaalatoom.
* Vorming van ionen:
* Metaal: Verliest een elektron en wordt een positief geladen ion (kation).
* Niet-metaal: Krijgt een elektron en wordt een negatief geladen ion (anion).
Voorbeeld: Denk aan de vorming van natriumchloride (NaCl):
* Natrium (Na): Een metaal met een lage elektronegativiteit.
* Chloor (Cl): Een niet-metaal met een hoge elektronegativiteit.
Wanneer natrium en chloor reageren, trekt chloor het gedeelde elektronenpaar sterker aan, waardoor effectief een elektron uit natrium wordt getrokken. Hierdoor blijft natrium over met een positieve lading (Na+) en chloor met een negatieve lading (Cl-), waardoor de ionische verbinding natriumchloride ontstaat.
Samengevat: Niet-metalen hebben de neiging elektronen op te nemen om een stabiele elektronenconfiguratie te bereiken. Daarom vormen ze anionen wanneer ze met metalen reageren.
 Is het feit dat er een combinatiereactie plaatsvindt tussen natrium- en chloorplekbaar voor argumentcombinatie van vormtafelzout?
Is het feit dat er een combinatiereactie plaatsvindt tussen natrium- en chloorplekbaar voor argumentcombinatie van vormtafelzout?  Wat gebeurt er met ionen nadat zout water verdampt?
Wat gebeurt er met ionen nadat zout water verdampt?  Convectie versus advectie:inzicht in de verschillende rollen van warmteoverdracht in vloeistoffen
Convectie versus advectie:inzicht in de verschillende rollen van warmteoverdracht in vloeistoffen  AI-gestuurd laboratorium versnelt katalyseonderzoek
AI-gestuurd laboratorium versnelt katalyseonderzoek  Kleine implantaten voor cellen zijn functioneel in vivo
Kleine implantaten voor cellen zijn functioneel in vivo
 NASA vindt tropische cycloon 02S consoliderend
NASA vindt tropische cycloon 02S consoliderend Watergebruik in de VS daalt tot niveaus die sinds 1970 niet meer zijn gezien
Watergebruik in de VS daalt tot niveaus die sinds 1970 niet meer zijn gezien Drakeneieren uitgebroed om vulkanische activiteit te volgen
Drakeneieren uitgebroed om vulkanische activiteit te volgen Valt zure regen altijd over het gebied dat fases produceerde of kan het op een afstand verderop?
Valt zure regen altijd over het gebied dat fases produceerde of kan het op een afstand verderop?  Andesgebergte:een tapijt van regenwouden, vulkanen en alpaca's
Andesgebergte:een tapijt van regenwouden, vulkanen en alpaca's
Hoofdlijnen
- Wat zou een persoon de mitochondria van de auto beschouwen?
- Wanneer organismen samenwerken om elkaar te helpen overleven, wordt het wat genoemd?
- Slim boksen:de eenvoudige conserveringsstrategie om bedreigde Roseate sterns te redden
- Wat maakt van een zenuwcel een dierencel?
- Hebben bacteriecellen een celmembraan?
- Wat worden granulocyten?
- Welke zin beschrijft een manier waarop meercellige en eencellige organismen hetzelfde zijn?
- Wat beschrijft het beste de interactie tussen DNA en RNA tijdens eiwitsynthese?
- Krijgen bacteriën voedsel en reproduceren zich zoals de manier waarop schimmels het doen?
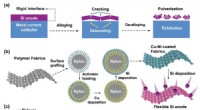
- Onderzoekers ontwikkelen biologisch afbreekbaar geprint display

- Wetenschappers stellen een flexibel interface-ontwerp voor een silicium-grafiet dual-ion batterij voor
- Elektronen versterken de calorische koeling in vaste toestand in hexagonale sulfiden

- Kleine magnetische deeltjes zorgen ervoor dat nieuw materiaal kan buigen, twist, en grijp

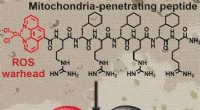
- Een metallopeptide richt zich op en verstoort de mitochondriale functie in stamcellen van borstkanker
 Wat is de relatie tussen cellen en organisme op een geheel?
Wat is de relatie tussen cellen en organisme op een geheel?  Calciumcarbide
Calciumcarbide Welk woord einde wordt geassocieerd met enzymen ASE en OSE?
Welk woord einde wordt geassocieerd met enzymen ASE en OSE?  Wat is de laagste laag van de atmosfeer van de aarde die direct boven de grond wordt genoemd?
Wat is de laagste laag van de atmosfeer van de aarde die direct boven de grond wordt genoemd?  Hoe wordt een cel geconstrueerd?
Hoe wordt een cel geconstrueerd?  Effect dat wattage zal hebben op een luidspreker wordt gedefinieerd als?
Effect dat wattage zal hebben op een luidspreker wordt gedefinieerd als?  Wat voor soort energie nuttig?
Wat voor soort energie nuttig?  Leven dinosaurussen nog?
Leven dinosaurussen nog?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

