
Wetenschap
Protonen in de organische chemie:rol, zuurgraad en basiciteit
1. Zuurgraad en basiciteit:
* Protonoverdracht: Protonen staan centraal in het concept van zuurgraad en basiciteit. Zuren doneren protonen, terwijl basen ze accepteren. De beweging van protonen tussen moleculen bepaalt de zuurgraad of basiciteit van een verbinding.
* pH-schaal: De pH-schaal, die de zuurgraad of alkaliteit van een oplossing meet, is gebaseerd op de concentratie van protonen (H+) in de oplossing.
2. Reactiemechanismen:
* Elektrofiele aanval: Bij veel organische reacties is sprake van een elektrofiele aanval, waarbij een elektron-deficiënte soort (elektrofiel) wordt aangetrokken door een elektronrijk centrum. Protonen kunnen fungeren als elektrofielen en deelnemen aan reacties zoals protonering van alkenen of alkynen.
* Nucleofiele aanval: Bij een nucleofiele aanval valt een nucleofiel (elektronenrijke soort) een elektrofiel aan. Protonen kunnen de reactiviteit van nucleofielen beïnvloeden, waardoor hun aanvalsvermogen wordt beïnvloed.
* Eliminatiereacties: Sommige reacties omvatten de verwijdering van een proton en een vertrekkende groep uit een molecuul, wat leidt tot de vorming van een dubbele of drievoudige binding. Protonen zijn essentieel voor deze eliminatiereacties.
3. Spectroscopie:
* Kernmagnetische Resonantie (NMR) spectroscopie: Protonen hebben een kernspin en zijn gevoelig voor het magnetische veld. NMR-spectroscopie maakt gebruik van deze eigenschap om verschillende soorten protonen binnen een molecuul te onderscheiden, waardoor waardevolle informatie wordt verkregen over de structuur van het molecuul.
4. Katalyse:
* Zuurkatalyse: Protonen kunnen fungeren als katalysatoren en reacties versnellen door de vorming van tussenproducten te vergemakkelijken of de activeringsenergie te verlagen. Veel organische reacties worden gekatalyseerd door zuren.
5. Structuur en hechting:
* Waterstofbinding: Protonen nemen deel aan waterstofbinding, een soort intermoleculaire interactie die cruciaal is voor de eigenschappen van veel organische moleculen. Deze interactie is verantwoordelijk voor het hoge kookpunt van water en de stabiliteit van DNA.
Voorbeelden:
* Zuur-base-reacties: Bij de reactie van een sterk zuur (zoals HCl) met water ontstaan protonen (H+). Deze protonen reageren met watermoleculen, wat leidt tot de vorming van hydroniumionen (H3O+), waardoor de oplossing zuur wordt.
* Elektrofiele additie: De toevoeging van HBr aan een alkeen omvat de protonering van het alkeen, waardoor een carbokation-tussenproduct ontstaat.
* NMR-spectroscopie: In het NMR-spectrum van ethanol (CH3CH2OH) verschijnen de protonen van de methylgroep (CH3) bij een andere chemische verschuiving dan de protonen van de methyleengroep (CH2). Dit verschil helpt bij het identificeren van de verschillende soorten protonen in het molecuul.
Concluderend spelen protonen een veelzijdige en onmisbare rol in de organische chemie, waarbij ze reacties, spectroscopie en de structuur van moleculen beïnvloeden. Het begrijpen van hun gedrag is cruciaal voor het begrijpen en voorspellen van de eigenschappen en reacties van organische verbindingen.
 Verbinding zorgt ervoor dat bacteriële communicatie door licht kan worden gecontroleerd
Verbinding zorgt ervoor dat bacteriële communicatie door licht kan worden gecontroleerd Wat is de elektronegativiteit van fenylsalicylaat?
Wat is de elektronegativiteit van fenylsalicylaat?  Wetenschapsprojecten met Borax
Wetenschapsprojecten met Borax  Hoeveel natrium in Kopenhagen?
Hoeveel natrium in Kopenhagen?  Waarom is de dichtheid van een stof in gasvormige toestand veel minder dan zijn vloeibare of vaste toestand?
Waarom is de dichtheid van een stof in gasvormige toestand veel minder dan zijn vloeibare of vaste toestand?
 De effecten van revolutie en rotatie op klimaat en weer
De effecten van revolutie en rotatie op klimaat en weer De midlifecrisis van de aarde - nieuw onderzoek ondersteunt de stilte in het geologische record
De midlifecrisis van de aarde - nieuw onderzoek ondersteunt de stilte in het geologische record Statistieken over extreme regenval kunnen veranderen naarmate het klimaat in de VS warmer wordt
Statistieken over extreme regenval kunnen veranderen naarmate het klimaat in de VS warmer wordt Welke dreiging vormt de watercyclus om zich voor te doen?
Welke dreiging vormt de watercyclus om zich voor te doen?  Ocean Habitat School Project
Ocean Habitat School Project
Hoofdlijnen
- Nieuwe ontdekking:gewone kwallen zijn eigenlijk twee soorten
- Hoe groeien organismen met veel cellen?
- Ideale omstandigheden voor bacteriegroei:voedingsstoffen, water en milieu
- Hoe wordt het genoemd wanneer het fenotype wordt bepaald door meer dan twee niet -gekoppelde loci?
- Wat zijn vooraf bevlekte eiwitten?
- Waar in een cel zou je enzymen zoeken?
- Hoe wordt het proces genoemd als er een embryo is gevormd?
- Welke structuur vertelt u dat Euglena getoont een autotrofe is?
- P53 (TP53) Tumor Protein: Function, Mutation
- Onderzoekers ontwikkelen draagbaar apparaat dat in 10 minuten 3D-afbeeldingen van de huid maakt

- Onderzoekers creëren aerogels met vormgeheugen met rubberachtige elasticiteit

- Nieuwe techniek brengt de studie van moleculaire configuratie in het microscopische domein

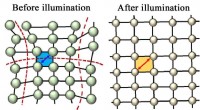
- Licht ontspant kristal om de efficiëntie van zonnecellen te verhogen
- Gemanipuleerde E. coli kan koolhydraten maken, hernieuwbare brandstof, van CO2

 Hoe is het terrein in Zuid -Korea?
Hoe is het terrein in Zuid -Korea?  Welke soorten energie worden gebruikt bij het fotograferen van een pijl?
Welke soorten energie worden gebruikt bij het fotograferen van een pijl?  Wat is het totale aantal atomen dat jodium pentachloride vormen?
Wat is het totale aantal atomen dat jodium pentachloride vormen?  Welk deel is niet van de wetenschappelijke methode?
Welk deel is niet van de wetenschappelijke methode?  Hoe koolstoflabels kunnen helpen in de strijd tegen klimaatverandering
Hoe koolstoflabels kunnen helpen in de strijd tegen klimaatverandering  Kracht nodig om een massa te versnellen?
Kracht nodig om een massa te versnellen?  Hoeveel Fahrenheit is 47 Celsius?
Hoeveel Fahrenheit is 47 Celsius?  Afbeelding:Cygnus-vrachtruimtevaartuig bij zonsopgang
Afbeelding:Cygnus-vrachtruimtevaartuig bij zonsopgang
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

